Questões de Concurso Público Petrobras 2012 para Técnico de Perfuração e Poços Júnior-2012
Foram encontradas 3 questões
Ano: 2012
Banca:
CESGRANRIO
Órgão:
Petrobras
Prova:
CESGRANRIO - 2012 - Petrobras - Técnico de Perfuração e Poços Júnior-2012 |
Q429126
Mecânica
A gasolina é um combustível fóssil e o seu calor de combustão é - 5.500 kJ/mol.
Considerando a gasolina constituída exclusivamente de C8 H18, o valor que mais se aproxima do calor máximo, em kJ, produzido pela queima de 1,0 L desse combustível é
Dados: densidade da gasolina = 0,7 kg/L
M (C8 H18 ) = 114 g/mol
Considerando a gasolina constituída exclusivamente de C8 H18, o valor que mais se aproxima do calor máximo, em kJ, produzido pela queima de 1,0 L desse combustível é
Dados: densidade da gasolina = 0,7 kg/L
M (C8 H18 ) = 114 g/mol
Ano: 2012
Banca:
CESGRANRIO
Órgão:
Petrobras
Prova:
CESGRANRIO - 2012 - Petrobras - Técnico de Perfuração e Poços Júnior-2012 |
Q429127
Mecânica
Um frasco de vidro contendo ácido sulfúrico de pureza analítica apresenta em seu rótulo as seguintes informações:
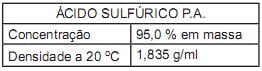
O volume aproximado, em mL, do ácido sulfúrico de pureza analítica necessário para o preparo de 1,0 L de solução aquosa do ácido com concentração 19,2 g/L é

O volume aproximado, em mL, do ácido sulfúrico de pureza analítica necessário para o preparo de 1,0 L de solução aquosa do ácido com concentração 19,2 g/L é
Ano: 2012
Banca:
CESGRANRIO
Órgão:
Petrobras
Prova:
CESGRANRIO - 2012 - Petrobras - Técnico de Perfuração e Poços Júnior-2012 |
Q429128
Mecânica
O enxofre contido no óleo combustível é lançado na at- mosfera na forma de SO2(g) quando este entra em combustão, conforme indicado na equação:
S(s) + O2(g)
Ao longo de um dia, os veículos de uma cidade queimam uma quantidade de óleo combustível contendo quatrocentas toneladas de enxofre.
Na hipótese de todo esse enxofre ser transformado em dióxido de enxofre, a massa, em toneladas, de SO2 lançada na atmosfera é
S(s) + O2(g)
→
SO2(g)Ao longo de um dia, os veículos de uma cidade queimam uma quantidade de óleo combustível contendo quatrocentas toneladas de enxofre.
Na hipótese de todo esse enxofre ser transformado em dióxido de enxofre, a massa, em toneladas, de SO2 lançada na atmosfera é