Questões de Química - Representação das transformações químicas para Concurso
Foram encontradas 1.436 questões
Na sequência, efetuou-se a filtração e o sólido não dissolvido foi separado e, depois de seco, medida a massa resultante.
A solubilidade do Ag2SO4 em água é 2,0×10–2 mol/L e sua massa molar é aproximadamente 312 g/mol.
Assinale a alternativa que indica corretamente a quantidade, em gramas, de sulfato de prata obtida após a filtração.
Com relação às reações químicas abaixo:
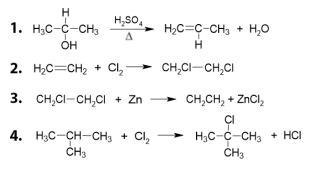
é correto afirmar que são, respectivamente, reações de
A fórmula estrutural deste antibiótico é mostrada a seguir:
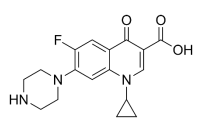
Com base na fórmula estrutural do ciprofloxacino, é correto afirmar que:
A fórmula estrutural desta substância é mostrada abaixo:
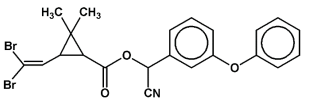
Sobre essa substância, é correto afirmar que:
CaCO3 + H3PO4 ➜ CaHPO4 + CO2 + H2O
Considere que se disponha de 100 kg de calcário (com teor de 90% em CaCO3) para reagir com ácido fosfórico (H3PO4) e formar fosfato bicálcico.
Qual a quantidade, em massa, de sal formado?
A solução de sulfato de cobre penta-hidratado possui 0,9988 g e a massa molar é 249,7 g/mol, já o KIO3 possui massa molar igual a 214,0 g/mol.
Qual a massa de KIO3, em gramas, necessária para que ocorra a precipitação?
Cu(s) + HNO3(aq) → Cu(NO3)2(aq) + NO(g) + H2O(l)
Balanceando-se a equação de oxirredução acima com algarismos inteiros, determina-se que o somatório de todos os seus coeficientes estequiométricos é igual a
( ) 1 unidade de H2O tem massa de 18,0 u e 1 mol de H2O tem massa de 18g.
( ) 1 unidade de CO2 tem massa de 56,0 u e 1 mol de CO2 tem massa de 56g.
( ) 1 molécula de NaCl tem massa de 68,2 u e 1 mol de NaCl tem massa de 68,2g.
( ) 1 molécula de NaCl tem massa de 58,5 u e 1 mol de NaCl tem massa de 58,5g.
( ) 1 unidade de CO2 tem massa de 38 u e 1 mol de CO2 tem massa de 38g.
Assinale a alternativa que aponta as corretas. Amedeo Avogadro postulou a hipótese de que volumes iguais de gases sob as mesmas condições de temperatura e pressão contém o mesmo número de constituintes. Com isto, o conceito de volume molar corresponde:
I - (Vm) é o volume ocupado por um mol de entidades elementares de uma substância.
II - A massa de uma substância é o mol dela mesma.
III - O volume molar pode se referir também ao volume da substância no estado sólido.
IV - O volume molar de qualquer gás nas CNTP é igual a 22,71 L/mol.
V - O mol é definido a partir do valor da massa atômica.
( ) Bronsted – Lowry = um ácido é um doador de prótons. ( ) Lewis = um ácido é um doador de par de prótons. ( ) Lewis = uma base é um aceitador de par de elétrons. ( ) Bronsted – Lowry = uma base é um aceitador de prótons.
Assinale a alternativa correta:
Considere as massas molares (g.mol-1 ):
Fe2O3 = 159,69; FeSO4 = 151,91; (NH4)2SO4 = 132,14.
A pureza (%) da amostra é, aproximadamente,
A reação química correspondente à decomposição de moléculas de água, produzindo moléculas das substâncias elementares hidrogênio e oxigênio, de conformidade com as Leis de Lavoisier e de Proust, é representada pela equação: 2 H2O → 2 H2 + O2.