Questões de Concurso
Foram encontradas 8.712 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Considere a reação abaixo e as afirmativas sobre ela, a seguir.
KMnO4 + H2SO4 + H2O2 → K2SO4 + MnSO4 + H2O + O2
I. A sequência correta dos coeficientes estequiométricos de cada uma das substâncias, na ordem em que elas aparecem na reação acima, é 2; 3; 5; 1; 2; 8; 5.
II. O KMnO4 se oxida e o H2O2 se reduz.
III. O KMnO4 ganha 5 elétrons e a H2O2 perde 2 elétrons.
IV. O KMnO4 é o agente oxidante e a H2O2 é o agente redutor.
V. A soma da carga dos reagentes é diferente da soma das cargas dos produtos.
Assinale a alternativa que apresenta a(s) afirmativa(s) correta(s).
Deseja-se preparar 250 mL de solução estoque de sulfato de amônio, com concentração de 10.000 µM de N-NH4+ , para tanto, deve-se pesar:
Dados: Massas atômicas (g mol-1) N= 14,01; H= 1,01; S= 32,07 e O= 16,00.
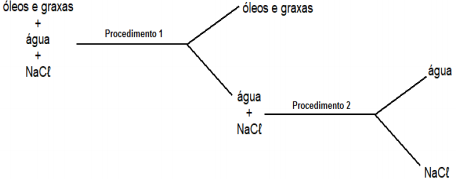
Sabendo que água e “óleos e graxas” são imiscíveis e o NaCℓ não é solúvel em “óleos e graxas”, assinale a alternativa que apresenta, na ordem, os dois procedimentos mais viáveis para separar uma mistura formada pelas três substâncias, segundo o esquema abaixo:
Considere a seguinte reação de hidrogenação de eteno, que acontece a quente e na presença de um catalisador em um reator, para responder a questão.
ETENO + H2 → X
A seguinte tabela apresenta informações acerca da energia, em termos de entalpia, de algumas ligações químicas.

Com base nessas informações, a entalpia da reação de hidrogenação de eteno é, em aproximadamente igual a
Considere a seguinte reação de hidrogenação de eteno, que acontece a quente e na presença de um catalisador em um reator, para responder a questão.
ETENO + H2 → X
Na seguinte tabela, são apresentados os dados referentes a três experimentos de combustão do monóxido de carbono, conduzidos à temperatura de 300 K, em atmosfera padrão.
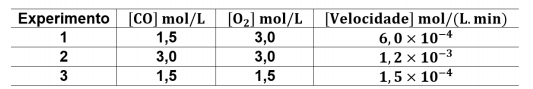
Com base nesses experimentos, a ordem global da reação é igual a
Em um procedimento analítico utilizando a técnica de cromatografia gasosa, um determinado analito apresentou um tempo de retenção de 10 minutos e a largura do seu pico na base foi igual a 2 minutos, como mostra o cromatograma na figura abaixo.
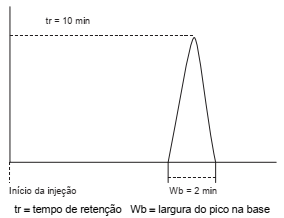
Com base nesses dados para o referido analito, o número de pratos teóricos da coluna é igual a:
Uma amostra de 50 mL de água contendo cátions Fe3+ foi tratada com excesso de NH4OH. O precipitado obtido depois de lavado, secado e calcinado pesou 0,320 g. A quantidade de ferro, em mol/L presente na amostra é
Dados:
Massas molares em g/mol
Fe = 56
O = 16
H = 1
N = 14
O volume, em mL, de ácido nítrico concentrado que deve ser diluído para a preparação de 500 mL de uma solução deste ácido de concentração 0,150 mol/L é igual a
Dados do rótulo do reagente concentrado:
Densidade d = 1,5 g/mL
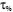 = 63% (massa/massa)
= 63% (massa/massa)
Massas molares em g/mol:
H = 1
N = 14
O = 16