Questões de Concurso
Foram encontradas 8.712 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
O p-nitrotolueno, um composto orgânico aromático, sofreu uma mono nitração após ser tratado com uma mistura de ácido nítrico e ácido sulfúrico, conforme descrito na figura que segue.
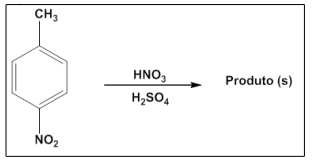
O número de produto(s) obtido(s) será igual a
Determinado composto orgânico foi submetido à análise química e a porcentagem de cada elemento químico que o constitui foi determinada. Os resultados estão apresentados na tabela a seguir.

Com base nas informações apresentadas, a fórmula mínima do composto é:
Considere os valores de entalpia padrão de formação de alguns compostos químicos apresentados na tabela a seguir.

Com base nas informações apresentadas, a variação de
entalpia, em kJ, para a reação de combustão completa de
um mol do gás propano (C3H8) é, aproximadamente:
Considere a reação hipotética X + Y ⇌ W, cuja velocidade de reação (v) foi determinada a partir das concentrações iniciais de X e Y, segundo os experimentos apresentados na tabela a seguir.
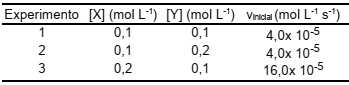
Baseando-se nos resultados apresentados na tabela, a
constante de velocidade de reação (k), em mol L-1 s-1
, é,
aproximadamente, igual a
A amônia pode ser preparada industrialmente pelo processo de Haber-Bosch, representado pela equação não balanceada a seguir.
N2(g) + H2(g) ⇌ NH3(g)
Supondo-se que a 300 ºC, esse experimento apresente concentração de N2 e de H2 de 0,3 e 2,0 mol L-1, respectivamente, e que a constante de equilíbrio Kc seja 10, a concentração de NH3, em mol L-1, nessa temperatura, deve ser, aproximadamente, de
O iodeto de hidrogênio pode ser preparado a partir do hidrogênio e do iodo moleculares na fase gasosa, conforme equação a seguir
H2(g) + I2(g) ⇋ 2HI(g)
Em um dado momento, pode-se determinar o seu quociente de reação (Qc), que representa a razão das concentrações iniciais dos produtos e dos reagentes. Nessa reação, se o valor encontrado de Qc for menor que o valor da
sua constante de equilíbrio (Kc), então,
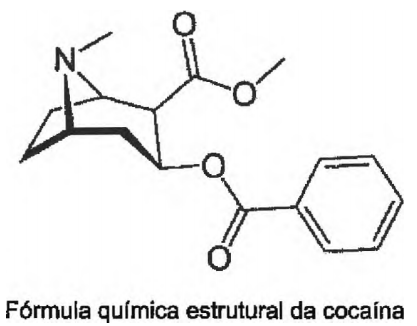
Um Perito Criminal Especial, ao realizar análise química qualitativa preliminar para identificação de cocaína, efetua as reações químicas descritas abaixo. Identifique a resposta que correlaciona corretamente a reação química com o princípio da técnica empregado.
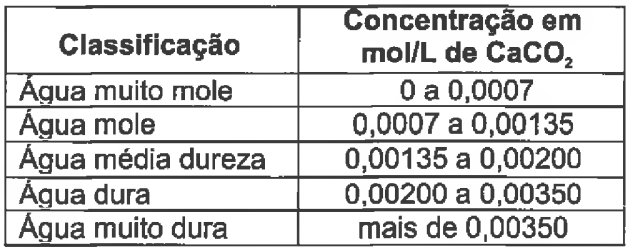
A dureza da água se define como a presença de íons di, tri e polivaientes, em especial, os íons Ca2+ e Mg2+. Um método que é comumente empregado para a determinação da dureza é acidificar uma amostra de água com HCI, levar à ebulição a solução ácida para eliminar o CO2 e neutralizá-la com NaOH. À solução se acrescenta solução tampão amoniacal até pH~10 e a solução resultante é titulada contra EDTA, utilizando-se o Negro de Eriocromo T como indicador para visualização do ponto final da titulação. A estequiometria do quelato EDTA com o metal é 1:1. Se uma amostra de água de 50,00 mL requer 15,00 mL de solução de EDTA 0,010 mol/L para alcançar o ponto final, esta pode ser classificada, segundo a tabela abaixo, como:
I. Remoção do solvente de ativação por um líquido similar à amostra (ex: água).
II. Aplicação da amostra (sorção ou retenção dos analitos).
III. Remoção de interferentes e parte da matriz com solvente que não remova os analitos (lavagem).
IV. Ativação do sorvente (resina ou suporte) com solvente apropriado.
V. Eluição dos analitos com um solvente apropriado.