Questões de Concurso
Foram encontradas 1.343 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
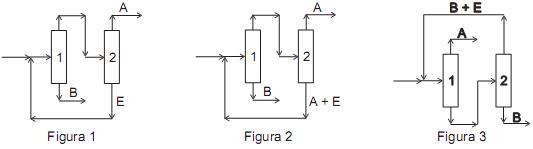
Observando o exposto acima, analise as afirmações a seguir, no que se refere ao comportamento dos azeótropos em relação à pressão.
I - A Figura 1 pode representar uma configuração em que A e B formam um azeótropo de máximo, e E não forma azeótropo.
II - A Figura 2 pode representar uma configuração em que A e B formam um azeótropo de mínimo, e E com A formam um azeótropo de máximo.
III - A Figura 3 pode representar uma configuração em que A e B, assim como E com B, formam um azeótropo de máximo.
É correto o que se afirma em
y = 0,73x + 0,27xD ,
sendo xD a fração molar do destilado.
A vazão de líquido na seção de esgotamento, em kmol/h, é, aproximadamente, igual a
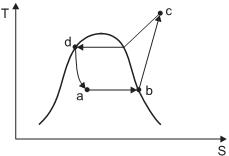
Se as entalpias dos pontos b, c e d são 3.500 kJ/kg, 5.000 kJ/kg e 500 kJ/kg, respectivamente, a vazão do fluido refrigerante (em kg/s) é de
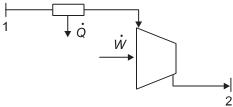
Desprezando-se as perdas de calor em outras etapas, a variação total de entalpia do fluido (em kJ/s e em módulo) no decorrer do referido processo é de

No fluxograma acima, vapor d’água superaquecido no estado 1, a 750 kPa e 650 °C (entalpia igual a -12.108 kJ/kg em relação à mesma referência da tabela de vapor d’água fornecida como anexo a esse caderno de questões), passa por uma válvula e em seguida por uma turbina, saindo do processo como vapor saturado a 82 °C, no estado 2.
Para uma vazão de vapor igual a 1 kg/s, a potência gerada pela turbina (em kW) é de
No sistema apresentado na Figura,
CO(g) + H2 O(g) ↔ CO2(g) + H2(g) (1)
Nessa temperatura, a constante de equilíbrio da reação assume o valor de K1 = 54,6. Além disso, a corrente de alimentação do reator contém água e monóxido de carbono na razão molar de 2:1, respectivamente.
Sabendo-se que a razão molar entre água e dióxido de carbono na saída do reator é de 1,035, a razão molar entre hidrogênio e monóxido de carbono na saída do reator é de
Sendo R a constante dos gases, o trabalho de compressão deste gás é dado por:
Mesmo assim, tal relação pode ser aplicada a processos irreversíveis, pois
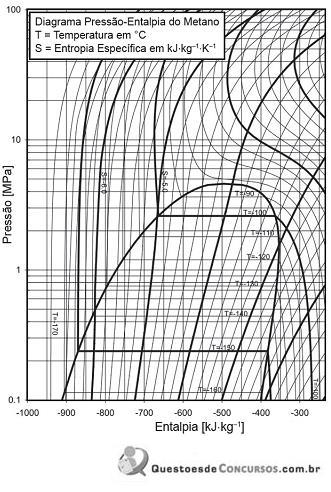
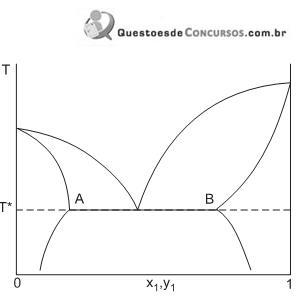
Metano líquido saturado a uma pressão de 0,7 MPa passa por uma expansão isotérmica até uma pressão de 0,2 MPa.
De acordo com o diagrama acima, a variação de entalpia nesse processo (em kJ/kg) é, aproximadamente, de
Neste contexto, a(s)
Assim, usando a relação de Maxwell correspondente, a variação de entropia (dS) T do sistema no referido processo é igual a
TANQUE 1: as vazões mássicas de entrada e de saída são iguais a W; o volume no tanque é V; e a temperatura da corrente de saída é ΔT superior à da corrente de entrada.
TANQUE 2: as vazões mássicas de entrada e de saída são iguais a W/2; o volume no tanque é 4V; e a temperatura da corrente de saída é 2ΔT superior à da corrente de entrada.
Para a manutenção dessas condições, as taxas de calor Q1 e Q2 cedidas pelos respectivos aquecedores elétricos dos tanques 1 e 2 são tais que
(hi representa a entalpia molar do composto i)
hCO(370 o C) - hCO(300 o C) = 2,2 x 103 J/mol
hH2O(370 o C) - hH2O(300 o C) = 2,6 x 103 J/mol
calor de reação a 370 o C ≈ -4 x 104 J/mol
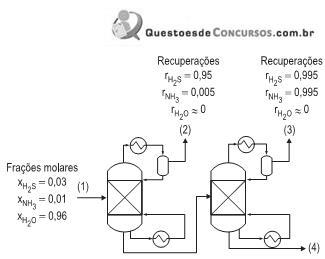
Um dos efluentes do processo de hidrotratamento de gás combustível é água contendo H2 S e NH3 , denominada água ácida. De forma a possibilitar a remoção de H2 S e NH3 , duas colunas de destilação são empregadas, conforme apresentado na Figura acima. As condições da entrada e recuperações dos compostos nas colunas estão apresentadas nessa Figura (as recuperações de água no topo das colunas são admitidas iguais a zero). A fração molar de H2 S que sai junto à água na corrente 4 é, aproximadamente, igual a
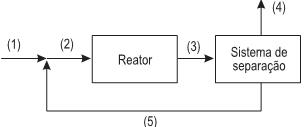
No processo ilustrado na Figura acima, operando em regime permanente, ocorre a reação R→ Produtos. Seja QR,i a vazão molar do composto R na corrente i.
Se Q R,5 /QR,3 é igual a 0,8, e a conversão de R por passe é igual a 0,5, a conversão global de R é, aproximadamente, igual a
A frações y2 e y3 e a vazão P são, respectivamente,
Se a vazão de vapor de água que entra com a corrente de ar na torre é 58 kmol . h-1 , a taxa de água evaporada na torre, em kmol .h-1 , é, aproximadamente, de
Dado Pressão de vapor de água a 41°C ≈ 0,08 atm
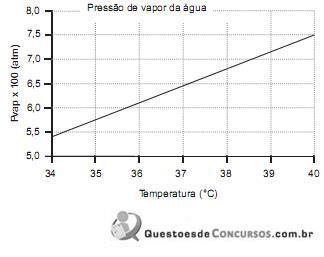
De acordo com o gráfico acima, a temperatura, em graus Celsius, de uma corrente de ar na pressão atmosférica com umidade relativa de 40% e 3% de água em base volumétrica é de, aproximadamente,
Dados
Massa molar da água = 18 g/mol
Massa molar do ar = 29 g/mol
Constante dos gases = 8,314 J/mol/K