Questões de Concurso
Foram encontradas 3.161 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
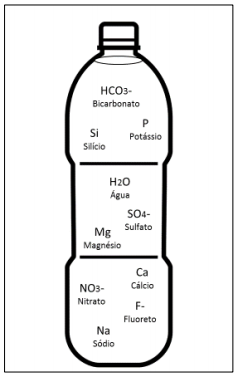
Em relação à água mineral e seus compostos, assinale a alternativa que apresenta a classificação química correta:
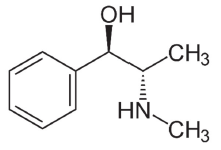
Na efedrina temos as funções orgânicas:
Qual a importância da CTC para os solos?
FeO(s) + CO(g) → Fe(s) + CO2(g) ∆H = x
Utilizando as equações termoquímicas abaixo e baseando-se na Lei de Hess,
Fe2O3(s) + 3 CO(g) → 2 Fe(s) + 3 CO2(g) ∆H = -25 kJ 3 FeO(s) + CO2(g) → Fe3O4(s) + CO(g) ∆H = -36 kJ 2 Fe3O4(s) + CO2(g) → 3 Fe2O3(s) + CO(g) ∆H = +47 kJ
Partindo de 1 tonelada de óxido ferroso a energia liberada será de aproximadamente quantos kJ?
I. CH3 – O –CH3 e CH3 – CH2 – OH. II. CH3 – CH = CH – OH e CH3 – CH2 – CHO. III. CH3 – NH – CH2 – CH2 – CH3 e CH3 – CH2 – NH – CH2 – CH3.
As isomerias que correspondem respectivamente a comparação dos compostos I, II e III são:
Dado o gráfico:
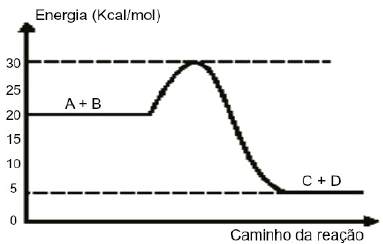
I. Trata-se de um processo exotérmico. II. A energia de ativação corresponde a 10Kcal/mol. III. O valor do complexo ativado é 30Kcal/mol. IV. A presença de um catalisador aumentaria a energia de ativação.
Estão corretas as afirmativas:
A substância apresenta a seguinte fórmula estrutural:
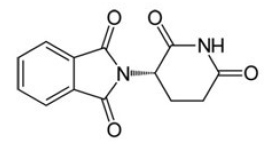
Sobre essa estrutura são realizadas as seguintes afirmações:
I. Apresenta 2 carbonos quirais. II. Tem a função amina na estrutura. III. A sua fórmula molecular é C13H10N2O4. IV. Não apresenta isomeria óptica.
Estão corretas as afirmativas:
A reação que ocorre é: Ag2S(s) + Aℓ(s)→ Aℓ2S3(s) + Ag(s)
Utilizando o processo descrito, a massa de prata metálica que será regenerada na superfície de um objeto que contém 5g de sulfeto de prata I é aproximadamente:
Sobre o metal mencionado no texto faz-se as seguintes afirmações:
I. Trata-se de um elemento representativo. II. Sua distribuição eletrônica é [Xe] 5p6 6s1 4f14 5d10. III. É isótopo do cátion bivalente platina. IV. Não pode ser oxidado por ser um metal nobre.
São corretas as afirmações:
Com relação aos símbolos químicos e seus significados, responda verdadeiro (V) ou falso (F) e assinale a alternativa que traz a sequência correta:
( ) - Sb – Seabórgio;
( ) - Cf – Califórnio;
( ) - Dy – Disprósio;
( ) - Lr – Lutécio;
( ) - Sc – Estrôncio.
Massas atômicas: H = 1; N = 14; O = 16.
C3H8 (g) + O2 (g) → CO2 (g) + H2O (l)
Considerando os dados apresentados na tabela a seguir, o calor de combustão (ΔH) de 0,5 mol de propano será:
Composto ΔHf° (kJ mol-1) C3H8 - 103,8 CO2 - 393,5 H2O - 285,8 Fonte: Novais (2016).
O sulfato de bário, substância muito utilizada em exames radiológicos, pode ser obtido por meio de uma reação entre o ácido sulfúrico e o hidróxido de bário, conforme reação equacionada a seguir:
Ba(OH)2(aq) + H2SO4(aq) → BaSO4(s) + H2O(l)
Considerando que a reação tem um rendimento de 80%, a massa, em gramas, de sulfato de bário obtido, quando são utilizados 0,05 kg de hidróxido de bário, será aproximadamente de:
Massas atômicas: H = 1; Ba = 137; S = 32; O = 16.
I - Água e óleo formam uma mistura heterogênea (líquidos miscíveis), pois uma substância praticamente não se dissolve na outra, podendo ser separadas pelo processo de decantação. II - Quando se coloca uma mistura de água e etanol no congelador, verifica-se que, sob pressão de 1 atm, o congelamento da mistura se inicia a uma temperatura abaixo da temperatura de fusão da água (0 °C). III - Para separar os componentes de uma mistura composta por água, etanol e pedra, podem ser utilizados os processos de filtração comum e destilação simples, respectivamente. IV - Uma mistura eutética se comporta como uma substância pura durante a ebulição, ou seja, apresenta temperatura de ebulição constante. V - A levigação é um método de separação de misturas, em que se utiliza água corrente para carregar os sólidos de baixa densidade, enquanto os mais densos permanecem depositados no fundo do recipiente. É usado pelos garimpeiros para separar o ouro do barro e da areia.
Assinale a alternativa com a sequência CORRETA.
Assinale a alternativa que indica as substâncias que são consideradas poluentes primários na formação da chuva ácida.