Questões de Concurso
Foram encontradas 3.161 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Considere as informações a seguir para responder à questão.
Na verificação qualitativa de íons iodato, IO-3 , foi realizado o teste com íons iodeto em meio ácido, segundo a equação não balanceada:
IO-3 (aq) + I-(aq) + H+(aq) → I2(s) + H2O(ℓ)
Para identificar a formação do I2 (s), toma-se uma alíquota da amostra após a reação, adiciona-se clorofórmio e agita-se. Ao final, se o iodo estiver presente, é observada coloração violeta rosada na fase orgânica.
Considere os seguintes valores de eletronegatividade de Pauling.
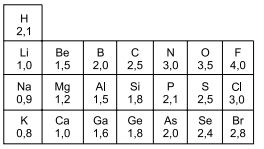
O caráter iônico é mais acentuado na ligação entre os
átomos de
− Hematita: Fe2O3; − Magnetita: FeO.Fe2O3; − Siderita: FeCO3; − Goethita: FeO(OH); e − Pirita: FeS2. É correto afirmar que
Dado: Volume molar de gás, nas CATP = 25 L/mol.
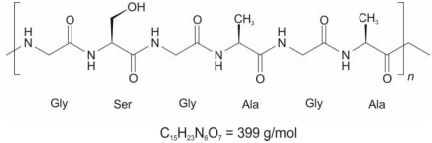
Nessa sequência de estrutura, a porcentagem em massa de nitrogênio é de
A fenolftaleína é um indicador ácido-base cuja faixa de viragem está descrita abaixo.
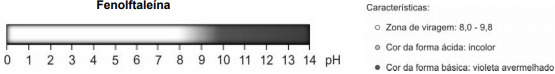
Espera-se observar a cor avermelhada ao colocar a fenolftaleína na solução resultante da mistura de água com
I. cloreto de amônio.
II. sódio metálico.
III. carbonato de sódio.
IV. sal de cozinha.
Está correto o que se afirma em
A estrutura abaixo representa a molécula de ibuprofeno, conhecido medicamento anti-inflamatório.
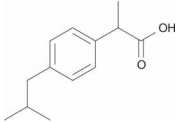
Essa substância reage com álcoois formando ...I... , porque pertence à função ...II.. .
Completam corretamente as lacunas I e II da frase acima:
Considere abaixo o equilíbrio químico.
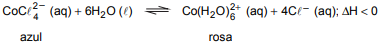
Em uma solução de cor rosa, espera-se observar a cor azul quando:
I. For adicionada solução de ácido clorídrico.
II. O sistema for aquecido.
III. Ao diluir a solução com água.
Está correto o que se afirma APENAS em
Considere o gráfico abaixo sobre a evolução da concentração de gás carbônico no ar.
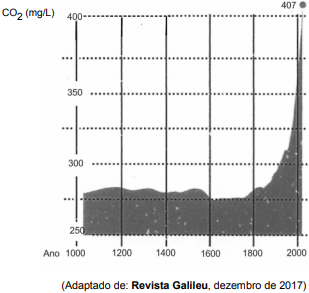
De acordo com o gráfico, do ano de 1600 até o último registro, a concentração de gás carbônico, em mol/L, passou de
(Adaptado de: Revista Galileu, dezembro de 2017)
Dados: Eletronegatividade de Pauling: O = 3,5 Si = 1,8 A composição do quartzo é SiO2. Assim, essa substância é formada por ligações
O composto orgânico de fórmula química
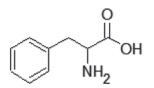
é conhecido como fenilalanina, um dos aminoácidos essenciais ao ser humano, e está presente em todas as proteínas animais e vegetais.
A fenilalanina também é encontrada em adoçantes sintéticos a base de aspartame. Sua nomenclatura segundo o sistema IUPAC é:
O gás natural transformou-se de sapo em príncipe na matriz energética mundial. No século XIX, nos Estados Unidos, era considerado um estorvo ao ser encontrado junto com o petróleo, pois exigia uma série de procedimentos de segurança que encareciam e complicavam as atividades de prospecção. No século XX, a partir dos anos 80, o consumo entrou em franca expansão e o gás natural transformou-se na fonte de energia de origem fóssil a registrar maior crescimento no mundo. Uma posição que detém até hoje e que deverá manter no médio prazo.
(ANEEL, Atlas de energia elétrica do Brasil. Capítulo 6 - Gás Natural, p. 93, acesso em abril de 2019).
Quanto ao gás natural, observe as assertivas abaixo.
I. O gás natural é um hidrocarboneto resultante da
decomposição da matéria inorgânica durante
milhões de anos.
II. O gás natural é encontrado no subsolo, em rochas porosas isoladas do meio ambiente por uma camada impermeável.
III. Em suas primeiras etapas de decomposição, esta matéria orgânica de origem animal produz o petróleo. Em seus últimos estágios de degradação, o gás natural. Por isso, é comum a descoberta do gás natural tanto associado ao petróleo quanto em campos isolados.
IV. Assim como ocorre no petróleo, a composição básica do gás natural são as moléculas de hidrocarbonetos encontradas em estado volátil e de baixa densidade.
A alternativa correta: é:
Segundo as normas técnicas referentes ao sistema de transmissão e distribuição de gás combustível, ABNT NBR 12.712, identifique a resposta correta:
I. Gás combustível é toda forma gasosa apropriada para uso como combustível doméstico, comercial ou industrial, sendo transmitida (transportada) ou distribuída para o usuário através de dutos.
II. A transmissão do gás (transporte) refere-se à atividade de transferência de gás combustível, por meio de dutos, desde as fontes de produção ou suprimento até os locais em que o produto passa para o sistema de distribuição de gás.
III. A distribuição de gás refere-se à atividade de fornecimento de gás combustível, por meio de dutos, aos estabelecimentos consumidores (residenciais, comerciais, industriais, outros) através de rede da companhia distribuidora.
IV. Gasoduto é uma tubulação destinada à transmissão e distribuição de gás.
A alternativa correta é:
Após uma aula experimental, o técnico de laboratório armazenou uma solução 0,015 mol L-1 de KMnO4 num recipiente de prata. Nesse contexto, considere os dados abaixo.
Dados:
E°(Ag+ /Ag0 )= 0,880 V e E°(MnO4- /Mn2+) = 1,510 V
∆G° = -n F ∆E° (sendo n o número de elétrons e F a constante de Faraday - 96450 C mol-1 )
Com base nesses dados e de acordo com os valores dos potenciais padrão de redução para
as duas semi-reações da célula eletroquímica, o recipiente de prata é
Um dado importante para avaliar a qualidade da água é a determinação do índice de dureza da água, que corresponde à presença dos íons Ca2+ e Mg2+. As equações envolvidas para essa avaliação são as seguintes:
Ca2+ + H2Y2- ⇋ CaY2- + 2H+
Ca2+ + MgY2- ⇋ CaY2- + Mg2+
Mg2+ + HIn2- ⇋ MgIn- + H+
MgIn- + H2Y2- ⇋ MgY2- + HIn2- + H+
O técnico do laboratório recebeu e protocolou uma amostra de água para análise de dureza. O volume da amostra utilizado na titulação foi de 100,0 mL, e o volume de solução de EDTA 0,0100 mol L-1 gasto na titulação foi de 25,0 mL. Considere o resultado expresso em mg de CaCO3 por 1000 mL e a classificação da dureza da água, presentes na tabela abaixo.

Com base nas equações e na tabela, essa amostra é classificada como água
Com relação à titulação de neutralização de um ácido fraco monoprótico por uma base forte, considere as afirmativas abaixo.
I No ponto de equivalência, o ácido fraco remanesce sem se ionizar.
II No ponto de equivalência, o pH será sempre maior que 7.
III Na metade do volume para o ponto de equivalência, o pH é igual ao pKa do ácido fraco.
IV Após o ponto de equivalência, o pH corresponde ao de uma solução tampão.
Das afirmativas, estão corretas