Questões de Concurso
Foram encontradas 3.161 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Uma amostra que pesa 1,55 g contém fósforo na forma de dihidrogenofosfato de sódio (NaH2PO4). Após receber tratamento adequado, a amostra foi misturada com solução de íons magnésio (Mg2+) e com solução de íons amônio, obtendo-se um precipitado de fosfato duplo de magnésio e amônio, conforme a reação a seguir:
H2PO4- + Mg2+ + NH4+ + 6H2O → MgNH4PO4 ˑ 6H2O(s) + 2H+
No procedimento de análise, o precipitado, após lavado e seco, foi decomposto a pirofosfato de magnésio (Mg2P2O7) conforme a reação abaixo.
2MgNH4PO4 ˑ 6H2O(s) 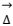 Mg2P2O7(s) + 2NH3(g) + 13H2O(g)
Mg2P2O7(s) + 2NH3(g) + 13H2O(g)
Se a massa de pirofosfato de magnésio obtida foi de 1,11 g, o teor de fósforo na amostra é
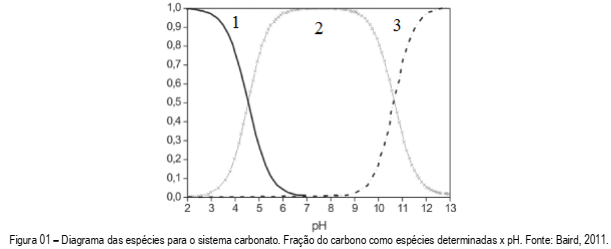
A química ácido-base de muitos sistemas de águas naturais, que inclui rios e lagos, é dominada pela interação do íon carbonato com o ácido carbônico, sendo o equilíbrio entre as espécies dependente do pH do meio. No gráfico abaixo, as espécies predominantes no sistema carbonato estão representadas por números 1, 2 e 3. Observando o gráfico, assinale a alternativa que correlaciona a numeração com a espécie, respectivamente.
O denominado potencial hidrogeniônico (pH) ou índice de Sorensen é usado para realizar a medida da concentração de íons H+ . O valor do pH para uma solução de HCl 0,5M, cujo grau de ionização é de 80%, é de:
Dado: log 2 = 0,3.
2g de uma mistura de sulfato de sódio e cloreto de potássio são tratados pelo nitrato de bário, obtendo-se um precipitado branco, que em seguida é lavado e seco e pesou 1,165g. A composição centesimal da mistura é:
Dados: Ba=137,33; Na=23,0; S=32,0; N=14,0; Cl=35,5 e K=39,0
O minério chamado “blenda” é utilizado na obtenção de zinco. Sabendo-se que uma amostra de tal minério contém 90% de pureza, a massa, em gramas, de zinco que pode ser obtida a partir de 200g de blenda é de:
Dados: Zn=65 e S=32.
A calcinação de 1,0 mol de sulfato de amônio formará quatro substâncias, sendo uma delas o gás amônia. A massa de gás amônia, em gramas, produzida na referida reação será de:
Dados: Ca=40; S=32; O=16 e H=1.
Uma solução contém 100g de açúcar C12H22O11 em 500g de água a 25°C. Sendo dado que a pressão de vapor da água pura a 25°C é de 23,76 mmHg, a pressão de vapor da solução é de:
Dado: C=12.