Questões de Concurso
Para química
Foram encontradas 13.095 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Considere os dados da tabela abaixo:

De acordo com os dados acima, o ânion que atua como base mais forte é:
Dados: log 2 = 0,3 e log 3 = 0,48
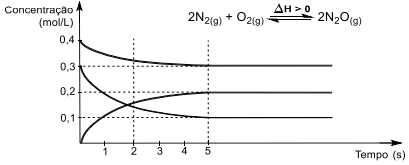
Sobre esse sistema reacional, é correto afirmar que:
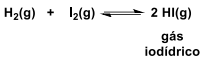
Considere um reator de 10L em que inicialmente são colocados 0,9 mol de H2(g) e 0,9 mol de I2(g) na temperatura T. Quando o equilíbrio for atingido, a concentração molar de HI(g) no equilíbrio será de:
Dado: log 3 = 0,48
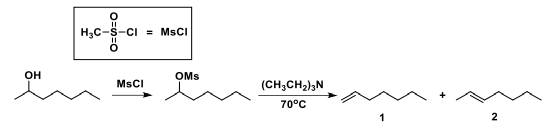
Sobre a etapa de eliminação, é correto afirmar que:
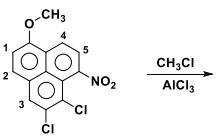
Na alquilação proposta acima, o grupo metil entrará preferencialmente na posição assinalada com:
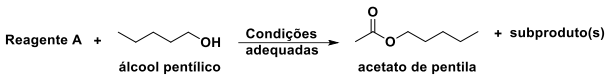
Considerando o esquema da reação acima, qual substância NÃO poderia ser utilizada como o “Reagente A”?
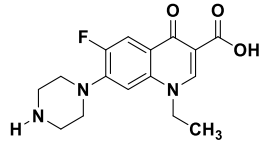
Nessa molécula NÃO está presente a função:
Massas molares em g/mol: C = 12; H = 1
1. O hidrocarboneto pode ser um alcano?
2. O hidrocarboneto pode ser um alqueno?
3. O hidrocarboneto pode ser um alquino?
4. O hidrocarboneto pode ser um alcadieno?
5. O hidrocarboneto pode ser um ciclano?
Os alunos que estiverem chegando a conclusões corretas responderão SIM apenas para o(s) questionamento(s):
1. pesou o objeto em uma balança analítica observando uma massa igual a 57,8499 g;
2. colocou 40,0mL de água em uma proveta;
3. mergulhou o objeto na água e observou a nova marcação do volume igual a 48,1mL;
4. pesquisou as densidades desses metais na literatura especializada:
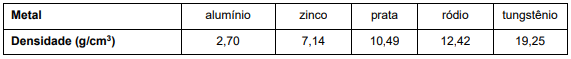
A partir desses dados, é possível concluir que o objeto é constituído de:
Massas molares em g/mol: C = 12; O = 16; Ca = 40
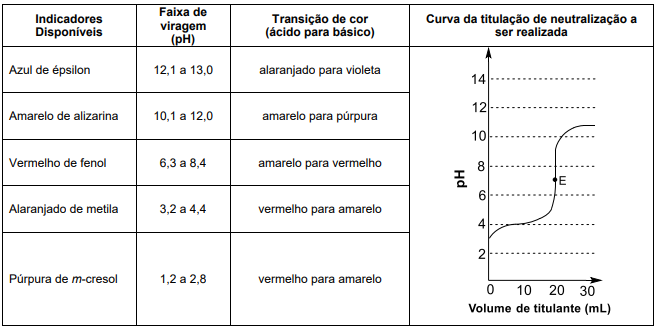
O indicador que o técnico deve utilizar é:

Nessa localidade há um rio em que ocorre despejo de efluentes industriais de uma empresa do ramo metalúrgico. Em um procedimento de fiscalização, uma amostra desse efluente foi coletada para análise e identificou-se a presença tanto de íons Cr2+ como de íons Hg2+ em concentrações de 1,0 x 10-3 g/L e 1,5 x 10-3 g/L, respectivamente. Considerando a densidade da amostra igual a 1g/cm3 , é correto afirmar que:
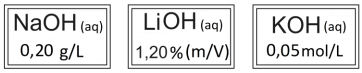
Considerando que todas as bases têm 100% de dissociação iônica e que o técnico precisa organizar as garrafas em ordem decrescente dos valores de pH, assinale a alternativa que indica a ordem correta das garrafas.
Massas molares em g/mol: H = 1; O = 16; Li = 7; Na = 23; K = 39