Questões de Concurso
Para química
Foram encontradas 13.134 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
I. Ar.
II. Sangue.
III. Granito.
IV. Madeira.
V. Gasolina.
VI. Soro fisiológico.
São exemplos de misturas heterogêneas o que se afirma apenas em
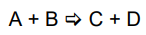
Observe a figura abaixo.
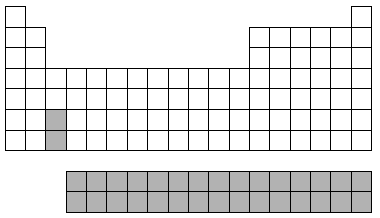
O modelo construído e proposto da figura agrupa os elementos químicos conhecidos e suas
propriedades e está organizado em ordem crescente de
I. A mistura de 5 g de soluto em 250 mL de água destilada resultará em uma solução 2% m/V.
II. O hidróxido de magnésio, vendido em farmácias para azia, é considerado como uma solução verdadeira e homogênea.
III. O ácido clorídrico é considerado um padrão primário, implicando que sua solução não requer análises para a determinação da concentração real.
Está correto o que se afirma apenas em
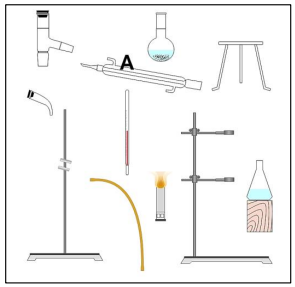
Sobre os processos de separação e, ainda, considerando disposto na imagem anterior, assinale a afirmativa correta.
C6H14 + O2 → CO2 + H2O
A massa de oxigênio necessária para reagir completamente com 2 mols de hexano será de, aproximadamente:
• Massa inicial da amostra de efluente: 50 g • Massa do papel de filtro utilizado: 0,5 g • Massa final do precipitado seco e papel de filtro: 3,8 g • Massa do reagente que precipitou: 0,8 g • Volume da amostra de efluente analisado: 0,5 L
Com base nessas informações, a concentração do contaminante no efluente em gramas por litro (g/L) é de, aproximadamente:
PbSO4 (s) ⇌ Pb2+(aq) + SO2–4 (aq)
A constante de equilíbrio (Kps) para essa reação é conhecida e equivale a 1,0 × 10−8 . Com base no equilíbrio iônico de solubilidade, a concentração máxima de íons de chumbo (Pb²⁺) na água tratada antes que o PbSO₄ comece a precipitar será de:
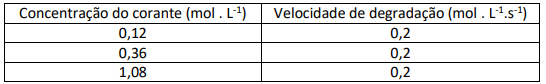
Os dados experimentais apresentados na tabela sugerem uma lei cinética de degradação de ordem: