Questões de Concurso
Para química
Foram encontradas 13.134 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
A partir dessas informações e considerando que MH = 1 g/mol, MC = 12 g/mol, e MO = 16 g/mol, que o volume molar de um gás ideal seja de 22,4 L e que todos os gases se comportem de forma ideal, julgue o item a seguir.
A instalação e a operação de tanques subterrâneos de
combustíveis requerem cuidados especiais para que se
evitem vazamentos, principalmente nos postos à beira-mar,
onde a proximidade da água salina pode acelerar o processo
de corrosão devido às reações de oxirredução.
Um exemplo clássico de uma reação química em
equilíbrio é a reação entre o monóxido de
nitrogênio (NO) e o dióxido de nitrogênio (NO): 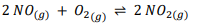
Nesta reação, o monóxido de nitrogênio (NO) reage com o oxigênio (O2) para formar dióxido de nitrogênio (NO2), e também ocorre a reação reversa, na qual o dióxido de nitrogênio (NO2) se decompõe para formar monóxido de nitrogênio (NO) e oxigênio (O2).
Assinale a alternativa que contém a equação para a constante de equilíbrio (KC) para esta reação.
Assinale a alternativa que cujas palavras ou expressões completam corretamente as lacunas da frase.
Observe a representação da estrutura química do paracetamol:
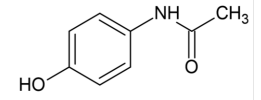
Quais grupos funcionais orgânicos estão presentes na estrutura química do paracetamol?
Qual é a distribuição eletrônica para o íon Co3+?
O petróleo é uma mistura complexa composta, em grande parte, por hidrocarbonetos. Julgue o próximo item, a respeito dos hidrocarbonetos.
Os hidrocarbonetos aromáticos, como o benzeno, são
compostos orgânicos em cuja estrutura há, pelo menos, um
anel benzênico.
Os hidrocarbonetos são compostos que consistem de apenas átomos de carbono e de oxigênio.
A estequiometria é aplicada em diversos estudos sobre a composição química de compostos e suas transformações químicas. No que se refere à estequiometria, julgue o item a seguir.
A estequiometria de uma reação apresenta a relação
qualitativa de reagentes formados e de produtos consumidos
nas diversas reações químicas indicadas por uma equação
química.
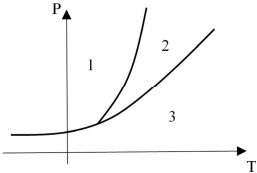
Na figura precedente, que corresponde ao diagrama de
fases de uma substância obtida a partir do fracionamento do
petróleo, as regiões 1, 2 e 3, delimitadas pelas curvas, estão
associadas aos estados físicos da substância, de acordo com as
condições de temperatura (T) e pressão (P).
Com base na figura e nas informações precedentes, julgue o próximo item.
A mudança de fase da substância do estado 1 diretamente
para o estado 3 corresponde ao que se denomina sublimação.
A respeito de transferência de calor, mudanças de estado e calorimetria, julgue o item que se segue.
Considere que a temperatura do petróleo extraído em uma
bacia terrestre seja igual a 110 °C. Nesse caso, se esse
petróleo for bombeado por meio de longas tubulações
metálicas até chegar aos tanques de armazenamento, o
petróleo não trocará calor com o meio externo.
Caso o petróleo extraído de um poço esteja armazenado em um tanque metálico por um tempo longo e suficiente para que esse petróleo esteja em equilíbrio térmico com as paredes do tanque e o meio externo, então, nessa situação, não haverá trocas de energia térmica entre o petróleo e o meio externo.
A respeito das reações de oxirredução e dos ensaios não destrutivos, julgue o próximo item.
Quanto mais eletropositivo um elemento for, maior será sua
tendência de ganhar elétrons.
A respeito das reações de oxirredução e dos ensaios não destrutivos, julgue os próximos itens.
A inspeção visual, ensaio não destrutivo, envolve a
observação direta da superfície do material.
Acerca de funções químicas, julgue o item a seguir.
Bases são caracterizadas pela liberação de íons OH−
e serão
tão mais fortes quanto mais estáveis forem suas fases não
ionizadas.
Acerca de funções químicas, julgue o item a seguir.
Os ácidos fortes são aqueles que se ionizam completamente
em solução aquosa, liberando todos os seus íons H+
, tendo
alta capacidade de doar prótons (íons H+
).
Acerca de funções químicas, julgue o item a seguir.
O potencial de neutralização de um ácido forte é maior em
um ácido fraco que em uma base forte.
Julgue o item a seguir, a respeito de dilatação térmica.
Para um material isotrópico, o coeficiente de dilatação
volumétrico (y) se relaciona com o coeficiente de dilatação
linear (a) por meio da equação 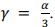
Uma estratégia que permite retirar as tampas metálicas de conservas de vidro é o resfriamento da tampa, se o coeficiente de dilatação linear da tampa metálica for superior ao do vidro.