Questões de Vestibular de Química - Termoquímica: Energia Calorífica, Calor de reação, Entalpia, Equações e Lei de Hess.
Foram encontradas 343 questões
O nitrato de potássio é um composto químico sólido, bastante solúvel em água, muito utilizado em explosivos, estando presente na composição da pólvora, por exemplo. Uma equação termoquímica balanceada para a queima da pólvora é representada abaixo:
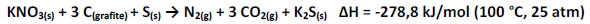
Assinale a alternativa que representa a interpretação correta da equação termoquímica para a queima da pólvora:
Considere a reação entre gás cloro e gás hidrogênio mostrada a seguir e ocorrendo em um sistema fechado:
Cl2(g) + H2(g) <-> 2HCI(g)
Dado: Constante dos gases (R) = 0,082 L.atm.mol-1.K-1.
Sobre esse processo, assinale a alternativa CORRETA:
Os efeitos globais gerados pela poluição advinda da queima de combustíveis fósseis tem levado à urgente necessidade por fontes alternativas de energia. Nesse contexto, o etanol (C2 H6O) e o gás hidrogênio (H2) emergem como possíveis substitutos da gasolina (C8 H18). A seguir estão apresentadas as reações de combustão de cada uma dessas espécies e os respectivos valores de entalpia padrão (25 ºC):
(Dadas as massas molares em g/mol: H=1, C=12, O=16)
C8
H18 + 12,5 O2 -> 8 CO2
+ 9 H2O
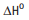 = –5471 kJ/mol
= –5471 kJ/mol C2
H6O + 3 O2 -> 2 CO2
+ 3 H2O
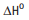 = –1368 kJ/mol
= –1368 kJ/mol H2
+ ½ O2 -> H2O
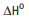 = –286 kJ/mol Com base nessas informações, pode-se afirmar que:
= –286 kJ/mol Com base nessas informações, pode-se afirmar que: H2CO3(aq) + Ca(OH)2(aq) → CaCO3(s) + 2 H2O(l) Equação 1
São apresentadas as entalpias-padrão de reação, em kJmol-1 , para três reações a 25oC:
I - CaO(s) + CO2(g) → CaCO3 (s) ΔH° = -183,3 kJmol-1 Equação 2 II - CaO (s) + H2O(l) → Ca(OH)2(aq) ΔH° = - 82,4 kJmol-1 Equação 3 III - CO2 (g) + H2O(l) → H2CO3(aq) ΔH° = - 20,5 kJmol-1 Equação 4
O valor da entalpia-padrão, em kJ, para a produção do carbonato na reação da equação 1 é:
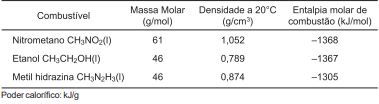
A tabela apresenta os valores de densidades, massa molar e entalpia molar de combustão de alguns combustíveis.
Considerando-se essas informações e com base nos conhecimentos de termoquímica, é correto afirmar:
