Questões de Vestibular Sobre termoquímica: energia calorífica, calor de reação, entalpia, equações e lei de hess. em química
Foram encontradas 343 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Um professor realizou um experimento em um laboratório no qual ele realizou a queima de papel amassado e de esponja de aço, respectivamente, em balanças artesanais, conforme figura 1.

I - Em ambas as combustões (queima do papel e queima da esponja de aço) são produzidos gás carbônico e Água.
II - A combustão da esponja de aço tem como produtos óxidos de Ferro.
III - A combustão do papel tem como produtos água e outros materiais.
Está(ão) correta(s) a(s) afirmativa(s):
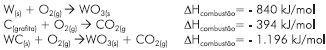
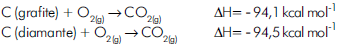
A quantidade de calor em kcal para efetuar a transformação de 2,4 kg de grafite em diamante é

De acordo com os estudos de Germain Henry Hess, professor da Universidade de São Petersburgo, no século XIX, a variação de entalpia em uma reação química depende apenas dos estados inicial e final de reagentes e de produtos da reação. A Lei de Hess contribuiu para o nascimento do princípio da conservação de energia.
A partir da aplicação da Lei de Hess, ao sistema de equações
termoquímicas I e II, é possível calcular a variação de entalpia
da reação representada pela equação química III.
Dessa forma, é correto afirmar: