Questões de Física - Física Térmica - Termologia para Concurso
Foram encontradas 1.041 questões
Um fio de cobre de 40 cm de comprimento e área de seção transversal desprezível, a uma temperatura inicial de 30 ºC (ou 18 ºX, em que ºX é outra escala termométrica), foi aquecido até atingir uma temperatura de 100 ºC (60 ºX).
Com base nessas informações, julgue o seguinte item, considerando o coeficiente de dilatação linear do cobre igual a 17 × 10-6 / ºC, e considerando também os princípios relacionados a escalas termométricas, equilíbrio térmico e dilatação térmica.
Após o aquecimento, o aumento sofrido pelo fio de cobre será
menor que 1 mm.
Em um calorímetro ideal, são colocados 100g de gelo a 0ºC e 100g de água a 50ºC que entram em equilíbrio térmico. Em seguida, é inserida no calorímetro uma massa M de alumínio a uma temperatura de 110ºC. A temperatura final de equilíbrio é 10ºC.
Considere:
Calor específico da água = 1,0 cal / goC. Calor específico do alumínio = 0,20 cal/ goC. Calor latente de fusão do gelo = 80 cal / g.O valor de M é
Considere que em uma brincadeira de colegas, eles sugam pela boca gás hélio e cantam parabéns para uma outra colega da turma.
A voz dos colegas se modifica, nesse caso, porque:
Considere que dois mols de um gás ideal monoatômico estão contidos em um dado recipiente que passa por uma transformação isobárica com pressão de 0,3 atm.
Nessa transformação, sua temperatura é elevada de 300 para 600 K e seu volume sofre uma elevação de 300 litros.
Assinale a alternativa que apresenta os valores mais próximos para a variação da energia interna, o trabalho realizado e a quantidade de calor trocada pelo gás,respectivamente.
(Considere R = 8,3 J/mol.K e 1 atm=1 x 10⁵ Pa)
Considere que em um experimento realizado em um laboratório de ciências, um estudante utiliza duas peças distintas metálicas, uma de alumínio e outra de ferro. Ele percebe que, ao fornecer a mesma quantidade de calor para ambas as peças, elas apresentam a mesma variação de temperatura.
Isso se deve ao fato, principalmente, de que:
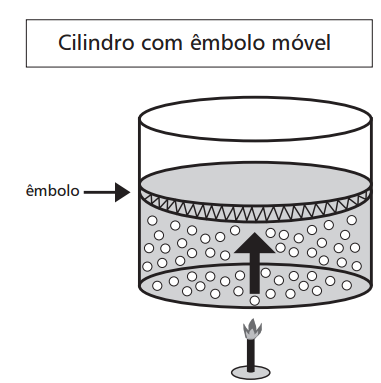
Em seguida, repetiram o experimento, provocando a mesma elevação de temperatura do gás, mas mantendo seu volume constante. A respeito do experimento, os estudantes formularam as seguintes conclusões: ( ) A variação da energia interna do gás foi a mesma nas duas situações. ( ) O calor fornecido ao gás, na primeira situação, foi igual ao fornecido na segunda. ( ) O trabalho realizado pelo gás foi maior na primeira situação.
Analisando as afirmativas acima, marque (V) para verdadeiro ou (F) para Falso. A sequência correta é
O estudo do calor e de suas transformações em energia mecânica é chamado de termodinâmica, que significa “movimento do calor”. A ciência da termodinâmica foi desenvolvida no início do século XIX, antes que a teoria atômica e molecular da matéria fosse compreendida.
P. Hewitt. Física Conceitual. 9.ª edição (com adaptações).
A respeito da termodinâmica, assinale a alternativa correta.
A figura mostra, em um diagrama p – V, a evolução de uma certa massa de um gás ideal, entre dois estados de equilíbrio térmico A e B.
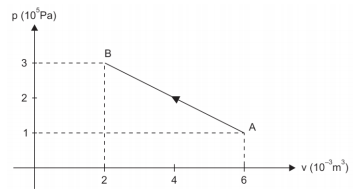
Considerando positiva a quantidade de calor trocada pelo gás com a vizinhança quando ela é recebida pelo gás, e negativa quando ela é cedida, a quantidade de calor que o gás trocou com sua vizinhança, ao evoluir de A até B, foi
O engenheiro francês Nicolas Léonard Sadi Carnot (1796-1832), cujo trabalho sobre máquinas térmicas viria a ser fundamental para que Rudolf Clausius e Lord Kelvin desenvolvessem a Segunda Lei da Termodinâmica, discutiu em seu trabalho de 1824 “Réflexions sur la Puissance Motrice du Feu” um ciclo idealizado para máquinas térmicas operando entre duas temperaturas, no qual a eficiência seria a máxima possível. Em sua homenagem, tal ciclo é chamado ciclo de Carnot.
Assinale a opção que melhor representa em um diagrama T – S
(temperatura – entropia) o ciclo de Carnot.
A respeito dos processos termodinâmicos a seguir, assinale V para a afirmativa verdadeira e F para a falsa.
( ) Em um processo adiabático de um gás ideal, a temperatura do gás se conserva constante, pois sem troca de calor não pode ocorrer variação de temperatura.
( ) Faz-se determinada massa de um gás ideal evoluir entre dois estados de equilíbrio termodinâmico. Tanto o trabalho W realizado pelo gás quanto a quantidade de calor Q, recebida pelo gás dependem do processo através do qual se deu a evolução entre os estados inicial e final de equilíbrio. Já a diferença Q - W é sempre a mesma, seja qual for o processo entre esses mesmos estados inicial e final.
( ) Deseja-se fazer a temperatura de determinada massa de um gás ideal sofrer um acréscimo ΔT cedendo-lhe calor. Para que a quantidade de calor cedida seja a menor possível, devemos aquecer o gás mantendo seu volume constante.
As afirmativas são, respectivamente,
A fusão durou