Questões de Concurso
Sobre transformações gasosas em física
Foram encontradas 90 questões
 Diante do exposto, sobre a energia, é correto afirmar que
o(a
Diante do exposto, sobre a energia, é correto afirmar que
o(aUm engenheiro inglês constatou que uma determinada massa gasosa ocupa um volume V0 a uma temperatura de –103 ºF. Posteriormente, ele observou que a pressão triplicou e a temperatura se elevou para 253,4 ºF. Ao calcular o volume final V da massa de gás no processo, o engenheiro constatou que:
Um engenheiro inglês constatou que uma determinada massa gasosa ocupa um volume V0 a uma temperatura de –103 °F. Posteriormente, ele observou que a pressão triplicou e a temperatura se elevou para 253,4 °F. Ao calcular o volume final V da massa de gás no processo, o engenheiro constatou que:
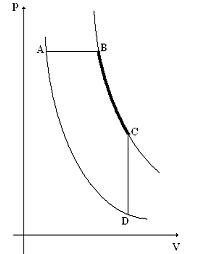
Assinale, entre as opções, aquele que representa corretamente essa mesma transformação.
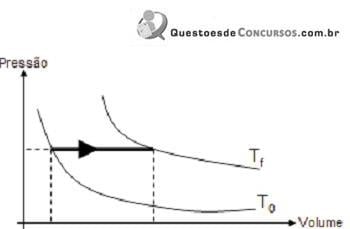
I. O diagrama representa uma expansão isobárica.
II. Como a pressão mantém-se constante, o trabalho é nulo.
III. O diagrama mostra que quando aumenta a temperatura ocorre o aumento da energia interna.
Em determinado momento, o êmbolo é bruscamente deslocado, por um agente externo, no sentido de comprimir o vapor até um volume menor; essa compressão gera uma combustão espontânea, transformando o vapor em gás, o que provoca, em seguida, um deslocamento do êmbolo até a posição inicial. O gráfico, da pressão (P) versus volume (V), que melhor representa a sequência de transformações ocorridas no interior do recipiente é
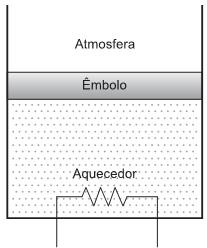
Em um determinado momento, o aquecedor é ligado, e o gás sofre uma expansão isobárica reversível até atingir o volume de 7,0 x 10-3 m3 , quando, então, o aquecedor é desligado.
Se a quantidade de calor total, entregue ao gás, foi de 500 J, qual foi, aproximadamente, em J, a variação da energia interna sofrida pelo gás?
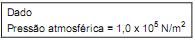
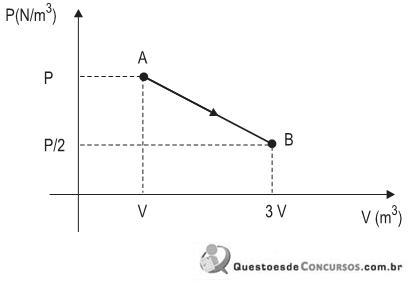
Um gás ideal realiza o processo térmico AB, conforme mostrado acima, partindo de um estado inicial A, com pressão P, volume V e temperatura T. O gás sofre uma expansão, e, no estado final B, a pressão do gás cai para P/2, e o volume aumenta para 3 V. Qual a temperatura final do gás em função da temperatura inicial T?
Dados: cp = 30 J/(mol•K) cv = 21 J/(mol•K)
Tal fato, conhecido como lei de Charles, é ilustrado pela figura
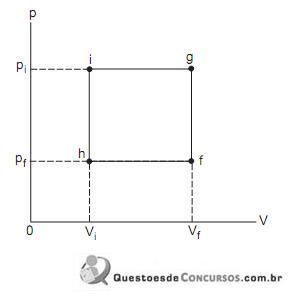
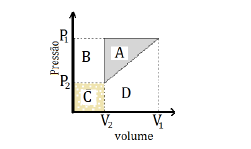
Observe o diagrama Pressão – Volume representado na figura acima. Quando um determinado sistema termodinâmico fechado é levado do estado inicial (i) para o estado final (f) através do caminho igf, 180 kJ são transferidos para dentro do sistema sob a forma de calor e 130 kJ são produzidos pelo sistema sob a forma de trabalho. Se o caminho percorrido for o ihf, o valor do trabalho produzido pelo sistema é 40 kJ. Com base nessas informações, a quantidade de energia (kJ) recebida sob a forma de calor pelo sistema, ao percorrer o caminho ihf, é

A figura acima ilustra o gráfico P×V do funcionamento de uma geladeira, que pode ser resumido nas seguintes etapas de um ciclo termodinâmico:
› no compressor, um gás, em geral CFC, é comprimido rapidamente, sem trocar calor, com elevação de pressão e temperatura. Não havendo troca de calor (Q = 0), o trabalho realizado pelo compressor equivale à variação de energia interna da substância;
› no radiador, ocorre diminuição de temperatura à pressão constante devido à troca de calor como o meio externo;
› a abertura da válvula de descompressão provoca uma descompressão rápida do gás, considerada adiabática. Nessa etapa, a pressão diminui e o volume aumenta;
› no congelador, o gás troca calor com o interior da geladeira à pressão e temperatura constantes. Devido ao processo de expansão, o gás retira calor do meio (interior da geladeira).