Questões de Concurso Comentadas sobre química
Foram encontradas 11.670 questões
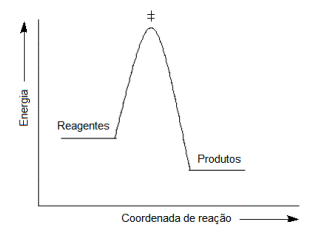
A reação esquematizada é classificada como:
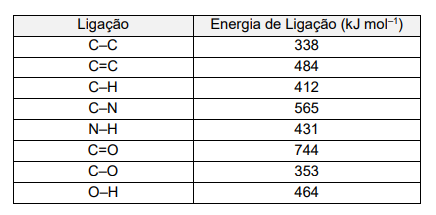
A tabela a seguir apresenta os valores de energias das ligações:
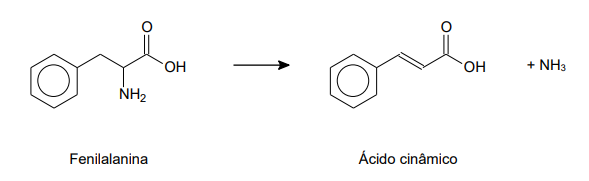
Utilizando os valores das energias das ligações fornecidos, a variação de entalpia envolvida na transformação da fenilalanina em ácido cinâmico representada, em kJ mol-1 , corresponde a:
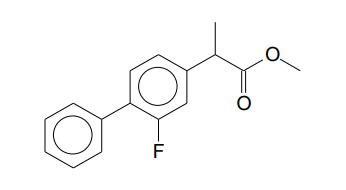
Considerando que o flurbiprofeno pode apresentar isômeros constitucionais e espaciais, a propriedade física utilizada para diferenciar os isômeros espaciais dessa substância é:
(MnO4) - (aq) + H2C2O4(aq) + H+ (aq) → Mn2+(aq) + H2O(l) + CO2(g)
A soma dos menores coeficientes inteiros que balanceiam a equação é:
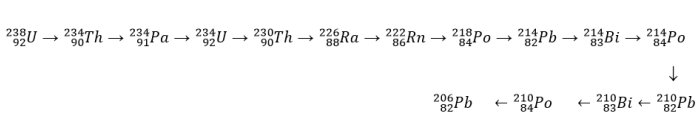
Nessa série radioativa de decaimento, a quantidade de partículas emitidas foi de:
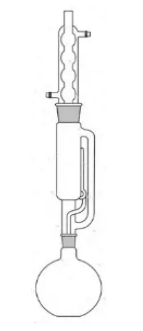
Essa aparelhagem é utilizada na técnica denominada: