Questões de Concurso Comentadas sobre química
Foram encontradas 7.317 questões
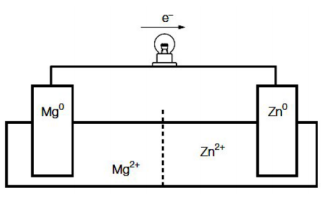
Sabendo-se que os elétrons fluem do eletrodo de magnésio para o eletrodo de zinco, é correto afirmar que
Fe2 (SO4 )3 + Cr2 (SO4 )3 + K2SO4 + H2O → K2Cr2O7 + H2SO4 + FeSO4
Na maioria dos laboratórios químicos, existem líquidos inflamáveis estocados. Para projetar ou
selecionar as instalações adequadas, as propriedades de cada produto, como: ponto de ebulição,
ponto de fulgor e tipos de extintores a serem instalados, devem ser conhecidas. Sobre ponto de
fulgor, assinale a alternativa correta.
I. A filtração a vácuo, também chamada de filtração por pressão reduzida, é utilizada para processos nos quais a filtração comum é demorada.
II. A filtração a vácuo utiliza, além da aparelhagem padrão da filtração comum, a adição de um funil de Buchner, de um kitassato e de uma trompa de arraste (trompa d’água).
III. A pipeta volumétrica é utilizada para medidas de volumes variáveis de líquidos.
IV. A bureta é utilizada para realizar medidas precisas de volume, sendo também utilizada em titulações.
1. Decantação. 2. Filtração. 3. Centrifugação. 4. Cristalização. 5. Destilação.
( ) Permite a separação de partículas de um sistema coloidal.
( ) Processo de separação baseado em pontos de ebulição diferentes.
( ) Processo de separação que se baseia em solubilidades diferentes.
( ) Ocorre a evaporação do diluente da solução saturada.
( ) Nas estações de tratamento da água, utiliza-se areia, pedra e carvão.
A concentração é uma característica importante para análise e interpretações de propriedades para as soluções e um dado necessário para seu uso no laboratório, na indústria e no cotidiano.
Abaixo, estão desenhados recipientes com os respectivos volumes de solução e massas de hidróxido de sódio (NaOH = 40g/mol).
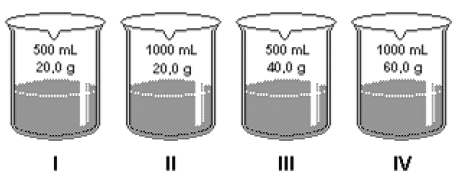
I. A solução contida no frasco I apresenta concentração de 1,0 mol/L;
II. As 4 soluções apresentarão pH acima de 7;
II. A solução mais concentrada está presente no frasco III.
São corretas as afirmações:
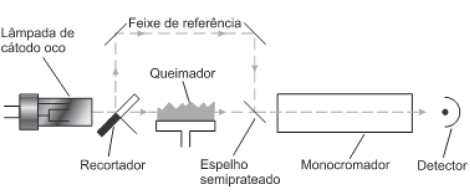
SKOOG, D. WEST, D. M. HOLLER, F. J. CROUCH, S. R Fundamentos de Química Analítica. 8 ed. São Paulo. Cengage Learning. 2010.
Ao considerar a instrumentação e os princípios da técnica analítica em si, analise as afirmações a seguir: I. A lâmpada de cátodo oco, consiste de um ânodo de tungstênio e de um cátodo cilíndrico selado em um tubo de vidro, contendo um gás inerte, como o monóxido de dinitrogênio. II. Como em toda a investigação relativa, há a necessidade de estipular um branco para a análise, já que no queimador podem surgir partículas que influem no sinal detectado e de natureza diferentes das que constituem a amostra analisada. III. A temperatura da chama é responsável pelas etapas de dessolvatação, vaporização e dissociação, bem como a conversão dos íons contidos na amostra em átomos neutros, estes últimos são os responsáveis por absorver o feixe de radiação.
É correto apenas o que se afirma em:
Um medicamento à base de ferro pode ter sua concentração conhecida por espectrofotometria UV/ Visível. Utilizando-se um medicamento de referência, realizaram-se as devidas diluições para a construção de uma curva de calibração. As medidas de absorbância, no comprimento de onda de absorção máxima de 510 nm, nas diferentes concentrações do medicamento de referência encontram-se na tabela a seguir:
Concentração (ppm) Absorbância
2,00 0,164
5,00 0,425
8,00 0,628
12,00 0,951
16,00 1,260
20,00 1,582
Os dados obtidos permitiram a construção de uma curva de calibração com coeficiente de correlação (R2) de 0,99978 e equação da reta: A = 0,01478 + 0,07812 x C. Sabendo-se que a absorbância da solução do medicamento à base de ferro foi de 0,715. Analise as propostas:
I. A concentração da amostra analisada é de 8,96 ppm.
II. O analito deve ser colorido, pois o comprimento de onda é na região do visível.
III. A absorbância está relacionada diretamente com a quantidade de radiação que atravessou a amostra analisada.
IV. A curva de calibração construída não se mostrou linear para o trecho estudado.
V. Se a amostra apresentar um valor de absorbância de 1,782 a concentração será de 22,60 ppm.
São corretas:
A análise quantitativa por espectrofotometria UV/Visível é muito utilizada para doseamento de determinados princípios ativos e corantes em formulações farmacêuticas disponíveis no mercado. Essa análise é confiável desde que obedeça a Lei de Beer, ou seja, a solução analisada deve obrigatoriamente seguir uma relação linear entre a absorbância e a concentração.
Considere a análise de um determinado fármaco que obedece a Lei de Beer. O que aconteceria com o valor de Absorbância se a concentração da solução do fármaco fosse o dobro? Considere que para esta análise utilizou-se uma cubeta de 1,00 cm de caminho óptico. O que aconteceria com o valor de Absorbância se uma nova medida fosse realizada com uma cubeta de 5,00 cm de caminho óptico?
O ácido perclórico P.A. apresenta concentração de 70%, sabendo que a densidade do ácido perclórico é 1,68g/cm-3 , assinale a alternativa que apresente o volume aproximado de solução do ácido que deve ser adicionado a um balão volumétrico de 200mL, afim de preparar uma solução 0,1 mol/L.
Dados M=100,46g.mol-1
Um cilindro contém uma mistura de 88 g de CO2(g) com uma quantidade desconhecida de gás argônio foi mantido em determinadas condições de pressão e temperatura.
Depois de vários testes, descobriu-se que com a adição de 220g de CO2(g) à mistura, mantendo-se temperatura e pressão constantes, o volume dobra.
Assinale a alternativa que apresenta a quantidade de argônio existente na mistura.
Dados: Massa atômica: Ar=40u; C=12u; O=16u

Qual é a concentração de íons sódio, em mol/L, presentes em 10g de cloreto de sódio dissolvidos em 50mL de água?
(Considere: MMNa=23g/mol, MMCI=35g/mol)
Considere a reação entre o ácido sulfúrico e o hidróxido de sódio e assinale a alternativa que apresenta a soma dos índices m, n, o e p.
mH2SO4(aq) + nNaOH(aq) oNas2SO4(s) + pH20(l)
[H2]=1,83x10-3 mol/L, [l2]= 3, 12x10-3 mol/L e [HI]= 17,67 X 10-3 mol/L. 2 HI(g)
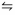 H2(g) + I2(g)
H2(g) + I2(g)