Questões de Concurso Comentadas sobre química
Foram encontradas 7.278 questões
A formação química da água, substância essencial para a vida, é composta por dois elementos químicos. Com base nessa descrição, assinale a opção que apresenta corretamente a composição molecular da água:
Considere uma reação do tipo A + B → C + D, sobre a qual foram coletados os dados abaixo:

Qual alternativa apresenta corretamente a ordem global e a constante de velocidade da reação?
A célula eletrolítica para purificação do cobre contém solução de sulfato de cobre (CuSO4), o material a ser purificado em um dos eletrodos e outro eletrodo onde se depositará o cobre puro, como representado a seguir:
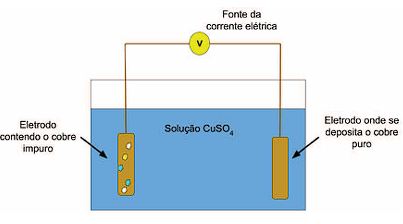
Disponível em: <https://www.saofranciscodeassis.edu.br/rgsn/arquivos/RGSN04/Refino-do-cobre-por-meio-daeletr%C3%B3lise-DAROSCI-OLIVEIRA-p171-182.pdf> (Com adaptações). Acesso em: 17 abr. 2024.
Sobre essa metodologia, é correto afirmar que:
Em uma aula de graduação para estudantes do curso de Química, é solicitado que os alunos obtenham furfural a partir de resíduo de cravo da índia. Para isso, o resíduo é tratado com ácido, e o material é submetido a uma destilação simples, onde o destilado contém o material de interesse.
Para isolar o furfural, os alunos devem realizar uma extração líquido-líquido. Em um funil de separação, adiciona-se o destilado aquoso e, em seguida, o solvente orgânico, no caso diclorometano. Após leve agitação, o funil é deixado em repouso e duas fases se formam, como representado na figura a seguir:
Dados:
Densidade da água = 1g/cm³
Densidade do diclorometano = 1,33 g/cm³
Coeficiente de distribuição: KD = Concentraçãofase orgânica/Concentraçãofase aquosa > 1
Sobre o procedimento descrito, qual das alternativas apresenta uma afirmação correta?
Em uma turma de Ensino Médio, o professor resolveu confeccionar uma bateria com materiais de baixo custo, para fins didáticos. Utilizando recipientes coletores, pregos galvanizados, pedaços de grafite e tintura de iodo contendo um pouco de iodeto de potássio, três células galvânicas foram montadas e associadas em série, como visto na figura abaixo:
Os alunos foram convidados a medir a tensão gerada pela bateria com auxílio de um multímetro.
DE ARAÚJO, Sayonara Maria Ferreira et al. Confecção de celas galvânicas com materiais de baixo custo para otimização de aulas sobre reações de oxirredução e eletroquímica no ensino médio. (Com adaptações).
Dados:
Potenciais de redução nas condições em que a bateria foi confeccionada:
I3- + 2e- → 3I- E = 0,53V
Zn+2 + 2e- → Zn E = -0,76V
Qual é o valor mais próximo do esperado para a bateria descrita?
Os gráficos abaixo são referentes a uma reação do tipo A → B + C.
No primeiro gráfico, temos a variação da concentração do reagente A em função do tempo de reação:
No segundo gráfico, temos a velocidade da reação em função do tempo:
Com base nos dois gráficos, o que é possível afirmar sobre a cinética da reação?
Em um laboratório químico, existem diversas vidrarias com diferentes funções e outras com funções similares, porém com diferentes níveis de precisão.
Assinale a alternativa que traz as vidrarias correspondentes à descrição a seguir:
São tubos calibrados que apresentam torneira, normalmente de teflon ou vidro. Capazes de dispensar volumes com precisão de acordo com a capacidade da vidraria.
Um químico observa que, durante a dissolução de um certo sal em água, o recipiente em que a solução está sendo preparada se resfria.
A explicação química mais coerente para esse fenômeno é:
Em um recipiente fechado, são adicionados hidrogênio e nitrogênio, ambos no estado gasoso. No recipiente são ajustadas as condições para que o material reaja segundo a equação abaixo:
Keq
3H2(g) + N2(g) ⇄ 2NH3(g)
Depois de atingido o equilíbrio, a concentração de hidrogênio (H2(g)) é igual a 0,34 molL-1, e a de amônia (NH3(g)) é igual a 0,44 molL-1.
Dados: Keq = 6,1 mol-2L2
Qual a concentração de nitrogênio (N2(g)) no equilíbrio?
Algumas substâncias podem ser obtidas a partir de diferentes matérias-primas submetidas às mesmas condições.
O composto X, por exemplo, pode ser obtido a partir de um aldeído, um éster ou um ácido carboxílico, como representado na figura abaixo:
A alternativa que contém a representação estrutural do composto X é:
Um técnico necessita preparar uma solução contendo ácido clorídrico e ácido acético em mistura, com concentrações de 0,05 mol/L e 0,06 mol/L, respectivamente.
No laboratório, ele dispõe de água destilada e um balão volumétrico de 500 mL, além das demais vidrarias necessárias. No almoxarifado, ele dispõe de soluções cujos rótulos estão representados abaixo.
Dados:
Massa molar do ácido clorídrico: 36,5 g/mol
Massa molar do ácido acético: 60 g/mol
Qual das opções a seguir apresenta os volumes corretos de cada ácido que o técnico deve usar para que obtenha a solução de que precisa?
O brometo de pinavério, cuja estrutura está representada abaixo, tem efeitos antiespasmódicos no músculo liso gastrointestinal e pode aliviar os principais sintomas da síndrome do intestino irritável. Esse medicamento é comercializado em comprimidos contendo 100 mg do princípio ativo.
Um analista dissolve completamente um comprimido de brometo de pinavério obtendo 200 mL de solução, depois toma 50 mL desse material e trata com solução de nitrato de prata, gerando massa de brometo de prata que se precipita no recipiente.
BOR, Serhat et al. Efficacy of pinaverium bromide in the treatment of irritable bowel syndrome: a systematic review and meta-analysis. Therapeutic advances in gastroenterology, v. 14, p. 17562848211033740, 2021. (usado com adaptações).
Dados:
Massa molar do brometo de pinavério: 591 g/mol
Massa molar do brometo de prata: 188 g/mol
Desconsiderando possíveis interferentes e impurezas e considerando que o nitrato de prata está em excesso, qual das alternativas é a mais próxima da massa de brometo de prata que foi formada?
Nos procedimentos de lavagens de vidrarias de laboratório, é comum incluir uma etapa de enxágue com um solvente que elimine tinta de canetas ou outros componentes com baixa solubilidade em água. O técnico do laboratório de Química Geral costuma usar etanol 92% (álcool etílico) nesse processo, mas está sem o produto, pois as entregas das compras atrasaram. Contudo ele possui as seguintes opções com boas quantidades no almoxarifado:
A |
B |
C |
|
|
|
|
D |
E |
F |
|
|
|
|
G |
H |
|
|
|
ATKINS, P.; JONES, L.; LAVERMAN, L. Princípios de química: questionando a vida moderna e o meio ambiente. 7 ed. Porto Alegre: Bookman, 2018. (material do professor, usado com adaptações)
Querendo o técnico usar um composto similar, quais opções disponíveis no almoxarifado apresentam a mesma função orgânica e, portanto, poderiam ser consideradas para substituir o etanol de lavagem?
Leia o texto para responder às questões de 32 a 34. Ao ser contratado, o técnico observou que foram acumulados, no laboratório, vários frascos com resíduos químicos que devem ser tratados e/ou encaminhados para descarte correto. Consultando uma central de resíduos já estabelecida, ele encontrou algumas informações que poderiam auxiliar nesse processo. Por exemplo, soluções aquosas de sais inorgânicos de metais alcalinos e alcalinos terrosos: NaCl, KCl, CaCl2, MgCl2, Na2SO4, MgSO4 e tampões PO43-, não contaminados com outros produtos, devem ser diluídos e descartados diretamente na rede de esgoto. Soluções de ácidos ou bases inorgânicas: H2SO4, HCl, H3PO4, HNO3, KOH, NaOH, Na2CO3, K2CO3, NaHCO3, KHCO3. devem ser diluídas e neutralizadas, podendo, então, serem desprezadas na rede de esgoto, desde que não contaminadas com outros produtos.
A primeira etapa foi a identificação dos frascos buscando segregar os resíduos que são passíveis de destruição /neutralização no próprio laboratório, para posterior descarte na pia. Três frascos foram separados, pois se enquadravam nessa situação. Eles estavam classificados como descrito abaixo:
Frasco | Quantidade | Composição sugerida |
1 | 9,6L | Resíduo da reação de H2SO412 mol L-1 com Magnésio metálico e água de lavagem. |
2 | 12,4L | Solução de Bicarbonato de sódio (NaHCO3) e Ácido clorídrico (HCl). |
3 | 11,2L | Resíduo de KOH 6 mol L-1 com água de lavagem. |
Prezando pela segurança, este técnico buscou confirmar o máximo de informações apresentadas nesses rótulos, antes de proceder a qualquer tratamento. Assim, ele realizou alguns ensaios com amostras dos resíduos de forma a verificar aspecto físico, coloração, presença de precipitados, pH e ainda testes qualitativos para íons.
Disponível em: <https://www.sgas.ufscar.br/degr/residuos/residuos-quimicos/tratamento-no-laboratorio> (Com adaptações). Acesso em: 17. Abr. 2024.
A composição indicada nos rótulos aponta que o frasco 1 contém uma substância ácida, a solução do frasco 2 apresenta um sal neutro enquanto a solução do frasco 3 apresenta uma substância de caráter básico.
Dentre as alternativas, qual apresenta uma substância ácida, neutra e básica, respectivamente, de acordo com a teoria ácido-base de Bronsted?
Leia o texto para responder às questões de 32 a 34. Ao ser contratado, o técnico observou que foram acumulados, no laboratório, vários frascos com resíduos químicos que devem ser tratados e/ou encaminhados para descarte correto. Consultando uma central de resíduos já estabelecida, ele encontrou algumas informações que poderiam auxiliar nesse processo. Por exemplo, soluções aquosas de sais inorgânicos de metais alcalinos e alcalinos terrosos: NaCl, KCl, CaCl2, MgCl2, Na2SO4, MgSO4 e tampões PO43-, não contaminados com outros produtos, devem ser diluídos e descartados diretamente na rede de esgoto. Soluções de ácidos ou bases inorgânicas: H2SO4, HCl, H3PO4, HNO3, KOH, NaOH, Na2CO3, K2CO3, NaHCO3, KHCO3. devem ser diluídas e neutralizadas, podendo, então, serem desprezadas na rede de esgoto, desde que não contaminadas com outros produtos.
A primeira etapa foi a identificação dos frascos buscando segregar os resíduos que são passíveis de destruição /neutralização no próprio laboratório, para posterior descarte na pia. Três frascos foram separados, pois se enquadravam nessa situação. Eles estavam classificados como descrito abaixo:
Frasco | Quantidade | Composição sugerida |
1 | 9,6L | Resíduo da reação de H2SO412 mol L-1 com Magnésio metálico e água de lavagem. |
2 | 12,4L | Solução de Bicarbonato de sódio (NaHCO3) e Ácido clorídrico (HCl). |
3 | 11,2L | Resíduo de KOH 6 mol L-1 com água de lavagem. |
Prezando pela segurança, este técnico buscou confirmar o máximo de informações apresentadas nesses rótulos, antes de proceder a qualquer tratamento. Assim, ele realizou alguns ensaios com amostras dos resíduos de forma a verificar aspecto físico, coloração, presença de precipitados, pH e ainda testes qualitativos para íons.
Disponível em: <https://www.sgas.ufscar.br/degr/residuos/residuos-quimicos/tratamento-no-laboratorio> (Com adaptações). Acesso em: 17. Abr. 2024.
Uma das propriedades relevantes dessas soluções que deve ser confirmada é o pH, que indicaria se a solução é ácida, neutra ou básica, como se espera para os frascos 1, 2 e 3, respectivamente. Essa medida de acidez e basicidade pode ser feita, qualitativa ou quantitativamente, no laboratório de Química usando diferentes equipamentos, vidrarias e/ou reagentes.
Das alternativas abaixo, qual apresenta as três possibilidades adequadas para estimar o pH das soluções?
Um dos tipos de extintores existentes é de CO2, preenchido por esse gás pressurizado. De forma simplificada, ele age diminuindo a concentração de oxigênio e assim extinguindo a chama, além de contribuir para o abaixamento da temperatura pela expansão do gás. Por conta disso, o manuseio desse extintor desse ser feito com cautela, pois esse gás atinge baixas temperaturas ao ser liberado.
Se um extintor operasse com as condições fictícias a seguir: 2kg de CO2, com um volume de gás pressurizado de 2,5L, operando a uma pressão de 27 MPa, qual temperatura em graus Celsius, o gás deve atingir ao ser liberado?
Disponível em: <https://www.extintoresporto.pt/conheca-o-extintor-co2-e-para-que-serve#:~:text=O%20difusor%20tem%20uma%20dupla,segura%20direcionada%20para%20as%20chamas.&text=No%20extintor%20de%20CO2%2C%20existe,do%20volume%20interno%20do%20recipiente>. (Com adaptações).
Acesso em: 17 abr. 2024.
Considere que o gás se comporta como um gás ideal; utilize R = 8,3 cm3 MPa K−1 mol−1; considere a relação Temp (K) = Temp (°C) + 273.
Um técnico do laboratório de Química encontrou um frasco sem rótulo com um metal desconhecido. Para descobrir que metal era esse, ele reagiu o mesmo com ácido clorídrico, obtendo a formação do gás hidrogênio, segundo a equação: M(s)+xHCl(aq)→MClx(aq)+H2(g)
Assim, ele montou um sistema para coletar o gás formado e utilizou um pedaço de metal de 0,09 g na reação; a temperatura ambiente era de 22ºC e a pressão atmosférica na cidade era de 0,91 atm. O técnico recolheu, no sistema montado, 36,5mL de gás hidrogênio.
Utilizando a equação dos gases ideais (p.V=n.R.T) e a fórmula da massa molar (MM=m/n), responda que metal deve ser esse.
Dados: T(K) = T(°C) +273. Constante dos gases (R) = 0,0821 L atm Mol-1 K-1 ou 8,206 x 10−5 m3 atm K−1 mol−1 ou 8,314 cm3 MPa K−1 mol−1 ou 8,314 L kPa K−1 mol−1.
Uma das atividades comuns no laboratório de Química da UNIFAL-MG refere-se ao preparo dos resíduos que são encaminhados para a correta destinação. Essa atividade é necessária, pois, muitas vezes, os alunos descartam, incorretamente, as substâncias usadas em aula, produzindo misturas que devem ser separadas antes da destinação final. Considerando que, no final da aula, os alunos descartaram tetracloreto de carbono (CCl4) junto às soluções aquosas, o técnico optou por separar a mistura por decantação.
Essa técnica é possível de ser usada graças à diferença de qual propriedade entre as substâncias?
Sobre ligações covalentes, é correto afirmar que:
Leia o texto a seguir para responder às questões de 21 a 23.
Alfenas está situada no Sul de Minas, às margens do Lago de Furnas, um dos maiores lagos artificiais do Brasil. Embora o objetivo inicial da construção desse lago tenha sido a geração de energia a partir da construção de uma usina hidrelétrica, ao longo destes 60 anos as atividades turísticas e recreativas se intensificaram nessa região e não é mais possível imaginá-la sem visitantes. Contudo, recentemente uma reportagem trouxe uma preocupação para a região. Um estudo da UFMG indicou que atividades humanas como a agricultura, pecuária e lançamento do esgoto in natura podem ter afetado a qualidade da água do Lago de Furnas. Em suas análises, a pesquisadora considerou dados oficiais de monitoramento das águas em Minas Gerais relativos às bacias que alimentam o Lago de Furnas, considerando os parâmetros de turbidez, pH, densidade de cianobactérias e os níveis de E. coli.
Quando nos referimos a contaminantes inorgânicos, como cromo, mercúrio, chumbo ou cadmio, a presença destes em fontes hídricas ou até mesmo nos peixes que ocupam essas fontes é comum, dadas as atividades cotidianas ou industriais que ocorrem nos municípios ao redor. E outra atividade frequente na região de Furnas refere-se à pesca esportiva ou como fonte de renda, com criação especialmente de tilápias em tanques. Embora não tenha sido apontado no estudo, o monitoramento constante dos níveis de contaminantes, sobretudo os inorgânicos, nas águas do lago, é crucial para garantir a qualidade do peixe que chega à mesa dos mineiros e seus visitantes.
Disponível em: <https://ufmg.br/comunicacao/noticias/presenca-de-contaminantes-fecais-no-lago-de-furnas-pode-estar-acima-do-permitido> (Com adaptações). Acesso em: 17 abr. 2024.
Chumbo (Pb) e Cromo (Cr) são dois contaminantes inorgânicos que merecem destaque dado o seu potencial tóxico e/ou carcinogênico. Diversos compostos desses metais são conhecidos e utilizados, dentre eles, CrCl3, PbO2, PbSO4, K2Cr2O7.
Considerando essas substâncias, qual alternativa apresenta a sequência correta para o estado de oxidação do Cr, Pb, Pb e Cr, nesses compostos, respectivamente?