Questões de Concurso Comentadas sobre química
Foram encontradas 7.278 questões
• Massa inicial da amostra de efluente: 50 g • Massa do papel de filtro utilizado: 0,5 g • Massa final do precipitado seco e papel de filtro: 3,8 g • Massa do reagente que precipitou: 0,8 g • Volume da amostra de efluente analisado: 0,5 L
Com base nessas informações, a concentração do contaminante no efluente em gramas por litro (g/L) é de, aproximadamente:
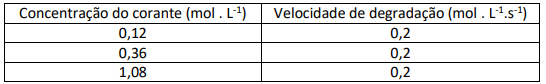
Os dados experimentais apresentados na tabela sugerem uma lei cinética de degradação de ordem:
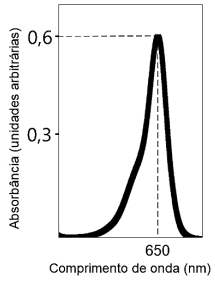
Considerando o espectro coletado e um coeficiente de absortividade molar de 40.000 L/(mol.cm) para o analito, a concentração da substância em µmol/L (micromol/L) determinada pela Lei de Lambert-Beer será de, aproximadamente:
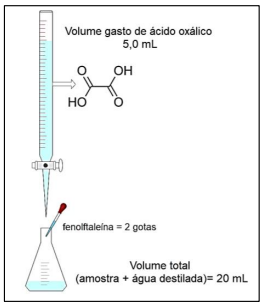
Considerando as informações fornecidas e a imagem, a concentração real da solução preparada de NaOH será de:
Assinale a alternativa que apresenta a quantidade de orceína a ser adicionada no preparo do corante.
Sobre o preparo dessa solução de HCl, assinale V (verdadeiro) ou F (falso) em cada afirmativa a seguir.
( ) Para o preparo da solução, serão necessários 84ml de HCl e 1000 ml de água destilada.
( ) Para evitar acidentes no laboratório, deve-se adicionar primeiramente a água destilada e posteriormente o HCl.
( ) Para uma medição precisa do volume da solução, deve-se utilizar um becker de vidro graduado, pois essa vidraria é mais precisa em relação aos balões volumétricos e às provetas.
A sequência correta é
Baterias de íon-lítio são um dos tipos de bateria recarregável mais amplamente utilizados na atualidade. A base de funcionamento desses dispositivos é a transferência de íons de lítio entre um catodo e um anodo. Em comparação com outras tecnologias, como níquel-cádmio ou níquel-hidreto, as baterias de íon-lítio apresentam maior densidade de energia, menor efeito de memória e menor perda de carga quando em uso.
A respeito das baterias de íon-lítio, julgue o item que se segue.
Em um modelo simplificado para uma bateria de íon-lítio
com anodo de grafite e catodo com substrato de cobalto
dopado com lítio, para descrever adequadamente o processo,
pode-se usar uma equação global do tipo
LiC6 + CoO2 ⮂ C6 + LiCoO2, cuja reação direta diz respeito
à descarga e a inversa, à carga.
Baterias de íon-lítio são um dos tipos de bateria recarregável mais amplamente utilizados na atualidade. A base de funcionamento desses dispositivos é a transferência de íons de lítio entre um catodo e um anodo. Em comparação com outras tecnologias, como níquel-cádmio ou níquel-hidreto, as baterias de íon-lítio apresentam maior densidade de energia, menor efeito de memória e menor perda de carga quando em uso.
A respeito das baterias de íon-lítio, julgue o item que se segue.
Para o mesmo peso, uma bateria de níquel-cádmio é capaz de
fornecer maior quantidade de watts x horas que uma bateria
de íon-lítio, mas em um intervalo de tempo maior.
Baterias de íon-lítio são um dos tipos de bateria recarregável mais amplamente utilizados na atualidade. A base de funcionamento desses dispositivos é a transferência de íons de lítio entre um catodo e um anodo. Em comparação com outras tecnologias, como níquel-cádmio ou níquel-hidreto, as baterias de íon-lítio apresentam maior densidade de energia, menor efeito de memória e menor perda de carga quando em uso.
A respeito das baterias de íon-lítio, julgue o item que se segue.
Às reações químicas que ocorrem nesse tipo de bateria
podem ser atribuídas constantes de equilíbrio.
Baterias de íon-lítio são um dos tipos de bateria recarregável mais amplamente utilizados na atualidade. A base de funcionamento desses dispositivos é a transferência de íons de lítio entre um catodo e um anodo. Em comparação com outras tecnologias, como níquel-cádmio ou níquel-hidreto, as baterias de íon-lítio apresentam maior densidade de energia, menor efeito de memória e menor perda de carga quando em uso.
A respeito das baterias de íon-lítio, julgue o item que se segue.
A maior densidade de energia apresentada por baterias de
íon-lítio significa que ela é capaz de descarregar mais
rapidamente, fornecendo energia a uma taxa superior.
Ao contrário de capacitores convencionais, que são preenchidos por dielétricos, supercapacitores eletrostáticos de dupla camada funcionam com um eletrólito entre os eletrodos. Ao se aplicar uma diferença de potencial entre os terminais do dispositivo, cátions aproximam-se da placa negativamente polarizada e ânions, da placa positivamente polarizada. Como resultado, a região interna fica distribuída da seguinte forma: o eletrodo positivo acumula uma camada de cargas negativas e o eletrodo negativo acumula uma camada de cargas positivas. A distância entre as placas e a película de carga é da ordem do tamanho do próprio íon correspondente.
A partir do texto precedente, julgue o item a seguir.
Embora apresentem uma menor densidade de energia do que
algumas baterias, supercapacitores usualmente têm maior
pico de densidade de potência.
Perovskitas são compostos que possuem fórmula química do tipo ABX3, em que A e B representam cátions de tamanho distintos e X representa um ânion. Um típico representante de ocorrência natural dessa classe é o mineral CaTiO3. Células solares baseadas em perovskitas já alcançaram eficiência superior a 25%. Apesar do enorme potencial para revolucionar o campo de energia solar, a implementação em larga escala de perovskitas ainda apresenta alguns obstáculos relativos à estabilidade e durabilidade desse material.
Com relação às perovskitas e sua utilização, julgue o item subsecutivo.
Nas células solares de junção dupla, ao se acoplar materiais
com gaps distintos, como perovskita e silício, concebe-se um
sistema que pode ser otimizado para coletar fótons de
diferentes energias.
Perovskitas são compostos que possuem fórmula química do tipo ABX3, em que A e B representam cátions de tamanho distintos e X representa um ânion. Um típico representante de ocorrência natural dessa classe é o mineral CaTiO3. Células solares baseadas em perovskitas já alcançaram eficiência superior a 25%. Apesar do enorme potencial para revolucionar o campo de energia solar, a implementação em larga escala de perovskitas ainda apresenta alguns obstáculos relativos à estabilidade e durabilidade desse material.
Com relação às perovskitas e sua utilização, julgue o item subsecutivo.
A sensibilidade de perovskitas em relação à radiação UV não
é um fator limitante do uso desse composto porque, em
células solares baseadas em perovskitas de haletos, o
material faz parte da camada de transporte, não participando
da absorção dos fótons característica do efeito fotoelétrico
Perovskitas são compostos que possuem fórmula química do tipo ABX3, em que A e B representam cátions de tamanho distintos e X representa um ânion. Um típico representante de ocorrência natural dessa classe é o mineral CaTiO3. Células solares baseadas em perovskitas já alcançaram eficiência superior a 25%. Apesar do enorme potencial para revolucionar o campo de energia solar, a implementação em larga escala de perovskitas ainda apresenta alguns obstáculos relativos à estabilidade e durabilidade desse material.
Com relação às perovskitas e sua utilização, julgue o item subsecutivo.
Uma perovskita de haleto é assim denominada por possuir
um haleto como um dos cátions, geralmente o menor.
Julgue o item que se segue, relacionados ao éxciton.
Um éxciton de Frenkel pode mover-se no interior de um
cristal, mas o elétron se mantém nas proximidades do
buraco.
Julgue o item que se segue, relacionados ao éxciton.
O aprisionamento de éxcitons na rede cristalina se dá
basicamente por três principais motivos: formação de
self-trapped éxcitons intrínsecos; formação de defeitos
(trapped ou bound éxcitons); e formação de self-trapped
éxcitons extrínsecos.
Julgue o seguinte item, a respeito da técnica de microscopia eletrônica de varredura.
Quando amostras não condutoras são submetidas à ação do
feixe de elétrons, ocorre o carregamento eletrostático da
superfície do material; em decorrência disso, podem ocorrer
contrastes irregulares, deformação e deslocamento da
imagem, e microanálises de regiões diferentes das
consideradas.
Julgue o seguinte item, a respeito da técnica de microscopia eletrônica de varredura.
Na microscopia eletrônica de varredura, os sinais emitidos
encontram-se sob a forma de elétrons e de fótons, os quais
são captados por detectores apropriados, sendo amplificados
e processados em um sistema analisador específico para cada
tipo de sinal.