Questões de Concurso Comentadas sobre química
Foram encontradas 7.275 questões
Com relação à Lei n.° 2.800/1956 e ao Decreto n.° 85.877/1981, julgue o item.
O número de conselheiros federais no Conselho
Federal de Química (CRQ) será renovado anualmente
pelo terço.
Sobre essa lei conclui-se que, para uma reação em meio gasoso, a constante de velocidade
Um dos objetivos principais dessa resolução é
Quando se comparam os dois tipos de petróleo e se consideram as características apresentadas, verifica-se que, em relação ao “petróleo pesado”, o “petróleo leve” apresenta
XCO3(s) → XO(s) + CO2(g)
Considerando-se a pureza do carbonato e a sua decomposição assumidamente completa, o elemento X em questão é o
6 Fe2+ (aq) + Cr2 O7 2+ (aq) + 14 H+ → 6 Fe3+ (aq) + 2 Cr3+ (aq) + 7 H2 O(l)
Com base nessas informações, a quantidade, em mol, de Fe2+ na solução de amostra é
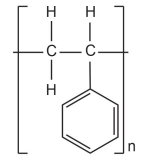
Com base na estrutura do monômero, a reação de polimerização para a formação do poliestireno é a
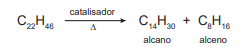
Ao se partir do alcano C30H62 , com formação de um alcano C12H26, a fórmula molecular do alceno produzido será
O grupo funcional detectado pelo teste com o reagente de Tollens e o resultado esperado dessa reação são os(as)
Quando se compararam os produtos obtidos em ambas as reações, constatou-se a formação de
Na Tabela a seguir, são apresentados três alcenos isômeros.
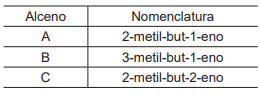
A representação em ordem crescente de energia liberada na combustão de 1 mol do alceno é a seguinte
Essa etapa tem como objetivo a(o)
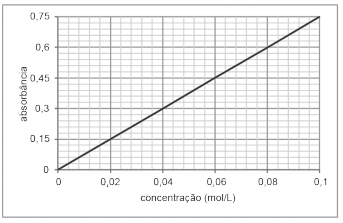
Uma amostra correspondendo a uma solução aquosa contendo Cu+2 passou pelo seguinte procedimento: uma alíquota de 10 mL dessa amostra foi completamente diluída em água até atingir um volume final de solução de 50 mL; uma alíquota dessa solução foi analisada no espectrômetro obtendo-se uma absorbância igual a 0,45.
A concentração de Cu+2 na amostra inicial, em mol L-1 , é
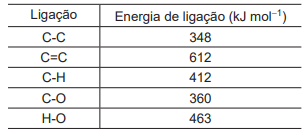
A variação de entalpia, em kJ mol-1 , da reação correspondente a esse processo industrial é
Nessa temperatura, o valor da constante do produto de solubilidade desse sal é, aproximadamente,
Nessa temperatura, o pKa desse ácido é igual a
Dado log 7 = 0,85
Dentre os ácidos formados pelo cloro, aquele que apresenta o menor grau de ionização corresponde ao
BrO3 - (aq) + 6 H+ (aq) + 6 e- → Br- (aq) + 3 H2 O (l) Eo red = +1,44 V
I2 (s) + 2 e- → 2 I- (aq) Eº red = +0,54 V
Em relação à pilha formada, observa-se que
I - C (s) + H2 O (v) → CO (g) + H2 (g) ∆H° = -28.000 cal mol-1 II - CO (g) + H2 O (v) → CO2 (g) + H2 (g) ∆H° = +9.400 cal mol-1 III - C (s) + 2 H2 O (v) → CO2 (g) + 2 H2 (g)
Considerando-se essas informações, a variação de entalpia, em cal mol-1 , da equação termoquímica III é
Nessa análise, a absortividade do analito, em L g-1 cm-1 , é