Questões de Concurso Comentadas sobre química
Foram encontradas 7.275 questões
Em relação aos processos eletroquímicos, julgue o item a seguir.
Toda célula eletroquímica é caracterizada por uma diferença
de potencial ou força eletromotriz que, em condições padrão,
é estimada a partir dos potenciais-padrão de redução de cada
semirreação, subtraindo-se o potencial-padrão de redução do
processo catódico do potencial-padrão de redução do
processo anódico.
Em relação aos processos eletroquímicos, julgue o item a seguir.
Na proteção catódica de dutos metálicos com base de ferro, o
duto é conectado mediante cabeamento elétrico a outro metal
mais fortemente oxidante, denominado de ânodo de
sacrífico.
Em relação aos processos eletroquímicos, julgue o item a seguir.
Toda reação eletroquímica pode ser decomposta em uma
semirreção de oxidação e uma semirreação de redução.
No que se refere às reações de oxirredução, julgue o item que se segue.
Oxidação é um processo que resulta no ganho de um ou mais
elétrons pelas substâncias, e redução é um processo que
resulta em ganho de dois elétrons pelas substâncias.
No que se refere às reações de oxirredução, julgue o item que se segue.
As seguintes equações são exemplos corretos de semirreações de oxirredução.
Ce+4 + e− → Ce3+
Fe+2 → Fe3+ + e−
Com relação às mudanças de estado físico da matéria e à calorimetria, julgue o item subsequente.
Se não existir matéria como meio de propagação, não é
possível a transferência de calor.
Com relação às mudanças de estado físico da matéria e à calorimetria, julgue o item subsequente.
A capacidade térmica de um corpo consiste na quantidade de
calor que ele necessita ceder ou receber para variar sua
temperatura em 1 grau, sendo diretamente proporcional
à sua massa.
Com relação às mudanças de estado físico da matéria e à calorimetria, julgue o item subsequente.
Além dos estados sólido, líquido e gasoso, há o plasma, que
é a condição da matéria associada a partículas muito
energizadas, com certo distanciamento e nenhuma ou pouca
ligação entre si, e cujas propriedades são semelhantes às do
estado líquido, mas com uma energia cinética maior.
Com relação às mudanças de estado físico da matéria e à calorimetria, julgue o item subsequente.
As mudanças de estado de líquido para gasoso podem ser
corretamente chamadas de evaporação, ebulição e calefação,
as quais se diferenciam principalmente pela velocidade em
que ocorrem.
Julgue o próximo item, relativo a propriedades dos hidrocarbonetos.
O estado de agregação de hidrocarbonetos (sólido, líquido ou
gasoso) está relacionado diretamente com a quantidade de
carbonos em suas cadeias, as quais, quando compostas por
mais de dezessete carbonos, resultam em substâncias no
estado sólido nas condições normais de temperatura e
pressão.
Julgue o próximo item, relativo a propriedades dos hidrocarbonetos.
Hidrocarbonetos são compostos insolúveis em água, por
serem praticamente polares, unidos por dipolo induzido.
Considerando que a estequiometria tem base em leis ponderais e compreende cálculos e regras para determinar a correta proporção das substâncias que se pretende utilizar, julgue o item a seguir.
Os coeficientes estequiométricos em uma reação química
podem ser determinados por tentativas; nesse caso, a fim de
melhorar a assertividade, são utilizadas algumas regras
empíricas, por exemplo, aquela em que se balanceiam, por
último, o carbono, o hidrogênio e o oxigênio, nessa ordem.

Disponível em: https://www.tabelaperiodica.org/
Considerando apenas a composição mencionada, a reciclagem dessas novas lâmpadas traria vantagens porque:
4 Au(minério) + 8 NaCN(aq) + O2(g) + 2 H2O(l) → 4 Na[Au(CN)2](aq) + 4 NaOH(aq)
A espécie química solúvel [Au(CN)2]− é posteriormente imobilizada sobre carvão ativado, e o ouro é recuperado por redução eletroquímica:
[Au(CN)2]−(aq) + e− → Au(s) + 2 CN−(aq)
Dados: Massa molar (g mol−1): Au = 197, NaCN = 49.
Considerando a estequiometria das reações, qual é a massa de ouro que se espera extrair, utilizando-se 1 kg de cianeto de sódio?
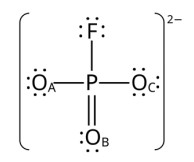
Ao se calcular as cargas formais de cada átomo na estrutura apresentada, conclui-se que são nulas, com exceção dos átomos:
A química orgânica e as características do carbono
Começou com a síntese da Ureia, A Química Orgânica que conhecemos; Com alguns grupos funcionais, E as propriedades que sabemos, E seu grande brilhantismo, Voltando-se para a pesquisa científica Que, independentemente do organismo, Descreveu um resultado inesperado, Contrariando a teoria do Vitalismo. (...) Compostos que ficaram conhecidos Como isômeros, para explicar O fenômeno isomeria é que dois Ou mais compostos venham apresentar. Diferente fórmula estrutural E mesma fórmula molecular
SOUSA, Mario Marques de. A Literatura de Cordel no Ensino de Química: uma Proposta Didática. In: Anais do 20º Encontro Nacional de Ensino de Química (ENEQ Pernambuco). Anais...Recife(PE) UFRPE/UFPE, 2020. Disponível em: http//www.even3.com.br/anais/ENEQPE2020.
Sabendo que a isomeria abrange boa parte dos estudos relacionados à Química Orgânica, assinale a alternativa que apresenta uma característica atribuída aos isômeros.
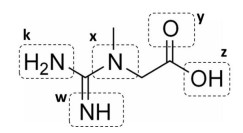
Em pH = 11,0, qual átomo estará carregado negativamente, formando uma espécie química iônica?
Considerando a estrutura química apresentada, assinale a alternativa correta.