Questões de Concurso Sobre química
Foram encontradas 13.580 questões
Analise as estruturas dos antioxidantes Rutina e Resveratrol abaixo.
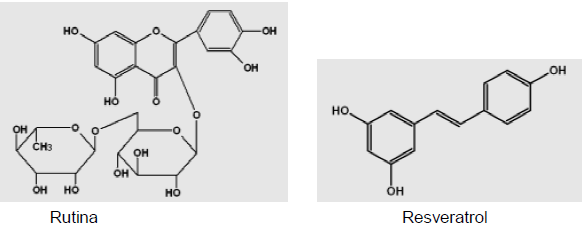
Acerca dessas duas moléculas, é CORRETO afirmar que
A busca por medicamentos anticancerígenos tem aumentado com vistas a se encontrar tratamentos mais efetivos e seletivos, ou que visem à descoberta de novas estratégias que impeçam o avanço da doença. O Taxol® faz parte de um grupo das substâncias mais atrativas e promissoras como anticancerígenas de aplicação clínica, para grande variedade de câncer.
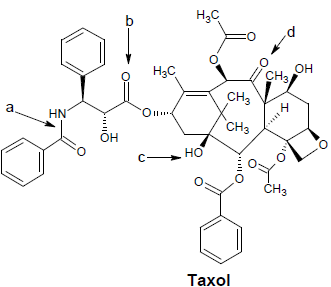
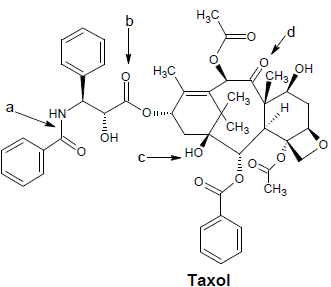
As funções orgânicas presentes no Taxol representadas pelas letras a, b, c e d, são
respectivamente:
NaHCO3 + HCl → NaCl + H2O + CO2
Podemos afirmar que o grau de pureza da amostra de bicarbonato de sódio é
A reação química em um bastão de luz ou pulseiras, em geral, envolve várias etapas diferentes. Um bastão de luz comercial é feito de uma solução de peróxido de hidrogênio e de uma solução contendo éster de fenil oxalato e um corante fluorescente. Acompanhe a sequência de acontecimentos quando as duas soluções são combinadas:
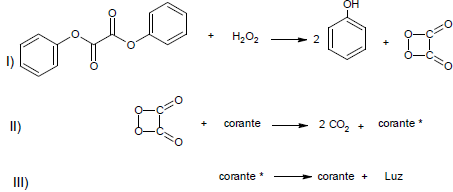
Considere as afirmativas abaixo:
I - O peróxido de hidrogênio oxida o éster de fenil oxalato, resultando em uma substância química chamada fenol e um éster de peroxiácido instável.
II - O composto de peróxi-cíclico se decompõe em dióxido de carbono; essa decomposição libera energia para o corante.
III - Os prótons dos átomos do corante migram para um nível mais alto, e depois retornam liberando energia na forma de luz.
ão CORRETOS:
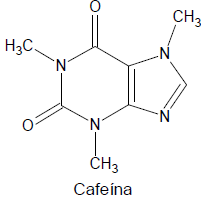
A fórmula molecular da cafeína é
O professor está programando a sua aula de titulação e precisa escolher qual o indicador ácido-base que usará para indicar o final da titulação entre solução aquosa de ácido clorídrico (titulante) e hidróxido de potássio. Dentre as opções que ele dispõe e que estão listadas abaixo, qual a melhor para esta titulação?
Indicador Zona de viragem
Violeta de metila (amarelo) 0,0 – 1,6 (azul-púrpura)
Azul de bromotimol (amarelo) 3,0 – 4,6 (violeta)
Alaranjado de metila (vermelho) 3,4 – 4,4 (amarelo)
Fenolftaleína (incolor) 8,2 – 10,0 (rosa)
Carmin de indigo (azul) 11,4 – 13,0 (amarelo)
100,0 g de carbonato de cálcio ultrapuro foram dissolvidos 1000,0 mL de água deionizada. Uma alíquota de 25,0 mL dessa solução foi titulada com solução 0,20 mol/L de ácido clorídrico. Qual o volume de HCl gasto, em mL, para titular completamente a solução de carbonato, sem excesso?
Dados: massa molar: C = 12 u; O = 16 u; Cl = 35,5 u; Ca = 40 U
Para proteger o ferro da corrosão, podemos utilizar outro metal que apresenta uma tendência maior a perder elétrons. Ele se chama de metal de sacrifício. Assinale a alternativa que apresenta o metal apropriado para tal, dentre os listados abaixo:
E0
Fe2+(aq) + 2e- → Fe (s) - 0,45
Zn2+(aq) + 2e- → Zn (s) - 0,76
Ni2+(aq) + 2e- → Ni (s) - 0,26
Sn2+(aq) + 2e- → Sn (s) - 0,14
Cu2+(aq) + 2e- → Cu (s) + 0,34
Indique, dentre os ácidos listados abaixo, aquele cuja base conjugada será a mais forte:
ácido Ka
Acético 1,75 x 10-5
Bórico 6,4 x 10-10
Benzoico 6,3 x 10-5
Lático 1,4 x 10-4
Oxálico 6,5 x 10-2
A água oxigenada, nomenclatura comercialmente conhecida, trata-se de uma solução aquosa de peróxido de hidrogênio (H2O2); que no comércio é encontrada geralmente em uma solução a 3%. Quando pura, é um líquido viscoso, de densidade 1,46 g/mL, incolor e de cheiro semelhante ao do ácido nítrico.Sua decomposição pode ser representada pela reação global: 2 H2O2 (aq) → 2 H2O (l) + O2 (g)
Esta reação ocorre em duas etapas, descritas a seguir:
Etapa 1 (lenta) H2O2 + I- → H2O + IO-
Etapa 2 (rápida) H2O2 + IO- → H2O + O2 + I-
Indique a alternativa que apresenta a lei de velocidade da decomposição do peróxido de hidrogênio.
O cloreto de magnésio tem sido muito usado como uma cura natural para muitos males do corpo humano. Ele pode ser obtido por meio da reação:
Mg (s) + 2 HCl (aq) → MgCl2 (aq) + H2 (g)
Quantos gramas de cloreto de magnésio podem ser obtidos quando 140 g de magnésio reagem com 355 g de ácido clorídrico?
Dados: massas atômicas: H = 1 u; Mg = 24 u; Cl, 35,5 u
“Cerca de 60% do nosso corpo é composto por água. Esse líquido precioso é fundamental para manter o sangue em circulação, controlar a temperatura e permitir inúmeras reações químicas que ocorrem a todo instante no organismo. Em dias normais, perdemos aproximadamente 2,5 litros de água pela respiração, pela urina, pelo suor e, em menor escala, pelas fezes. Claro que no verão ou após uma atividade física intensa, a perda pode ser maior.” Indique a alternativa que apresenta o número de átomos de oxigênio que são perdidos pela respiração, de acordo com o texto acima.
Dados: massas atômicas: H = 1 u; O = 16 u; N =; dágua = 1,0 g/mL 6,0 x 1023