Questões de Concurso Sobre química
Foram encontradas 13.584 questões
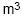 contém gás perfeito à temperatura de 27° C e à pressão de 996 Pa. O número de moléculas do gás no recipiente é
contém gás perfeito à temperatura de 27° C e à pressão de 996 Pa. O número de moléculas do gás no recipiente é
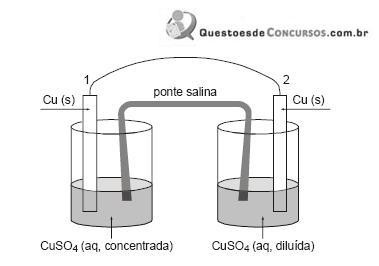
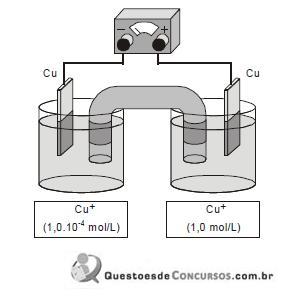
Durante o funcionamento dessa pilha eletroquímica, antes de atingir o equilíbrio, observa-se:
I. fluxo de elétrons de 1 para 2.
II. reação de redução do
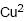 + em 2.
+ em 2. III. aumento da massa da placa de Cu (s) em 1.
É correto o que se afirma APENAS em

As lacunas são preenchidas corretamente por, respectivamente,
I. O aumento da temperatura global média tem sido proporcional ao aumento do dióxido de carbono encontrado na atmosfera.
II. Entre os gases responsáveis pelo efeito estufa, encontra- se o dióxido de carbono, óxido nitroso e o metano.
III. O vapor de água presente na atmosfera também contribui para o efeito estufa.
IV. A queima de combustíveis fósseis contribui para o aumento do efeito estufa
V. Se não existissem gases presentes na atmosfera causadores do efeito estufa, a temperatura da superfície do planeta seria muito baixa impossibilitando a existência de vida na forma que conhecemos.
I. Tanto as moléculas de sabão como as de detergente reagem com as gorduras quebrando a cadeia carbônica destes compostos e, desta forma, aumentando sua solubilidade em água.
II. A diferença entre detergentes sulfonados biodegradáveis e não-biodegradáveis são as estruturas das cadeias laterais, enquanto que no detergente biodegradável esta cadeia é linear, no detergente não biodegradável esta cadeia é ramificada.
III. Tanto as moléculas dos detergentes como as dos de sabões possuem uma parte hidrofílica e uma parte hidrofóbica.
IV. Na reação para a obtenção de sabão comum, os glicerídeos (gorduras de fonte animal) reagem com soda cáustica produzindo glicerol mais o sabão propriamente dito.
V. As moléculas de sabões e detergentes formam micelas com superfícies hidrofóbicas.
É correto o que se afirma APENAS em
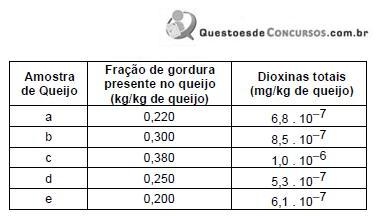
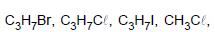
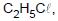 em ordem crescente de ponto de ebulição são:
em ordem crescente de ponto de ebulição são:1.
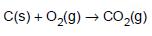
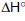 =-393,5kJ/mol
=-393,5kJ/mol2.
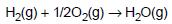
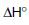 =285,8kJ/mol
=285,8kJ/mol3.
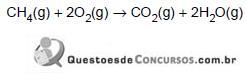
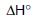 =-890,3kJ/mol
=-890,3kJ/mol4.
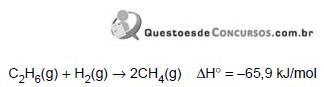

Estão corretas as associações:
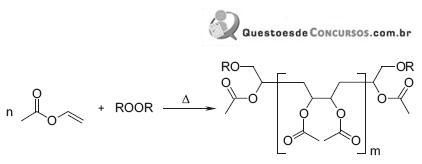
Em relação a este processo, é correto afirmar que
I - Copolímeros consistem em uma mistura física de dois homopolímeros compostos por monômeros estruturalmente diferentes, normalmente pela mistura de soluções dos dois polímeros, seguida da evaporação do solvente.
II - Copolímeros podem ser obtidos pela reação entre diferentes monômeros, sendo que a proporção relativa entre eles na estrutura do copolímero dependerá de suas reatividades químicas.
III - Copolímeros, por possuírem mais de um monômero, apresentarão as propriedades físicas e químicas dos homopolímeros, combinadas em um único material.
É(São) correta(s) APENAS a(s) afirmativa(s)
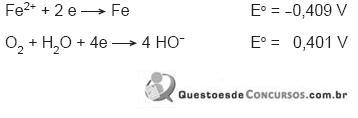
Considerando que a variação de energia livre de uma reação de oxidorredução pode ser calculada pela fórmula
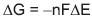 , na qual n é o número de elétrons transferidos, F é a Constante de Faraday
, na qual n é o número de elétrons transferidos, F é a Constante de Faraday 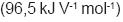 e
e 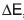 , a diferença entre os potenciais padrão das reações de oxidação e de redução, conclui-se que a(o)
, a diferença entre os potenciais padrão das reações de oxidação e de redução, conclui-se que a(o)I - Um balão cheio com 1 L de gás carbônico
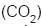 não flutua, mas murcha, porque o
não flutua, mas murcha, porque o 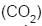 é mais denso do que o ar.
é mais denso do que o ar. II - Um balão cheio com hélio flutua porque este gás, apesar de ser mais denso do que o ar, possui menor volume molar, devido ao seu menor raio atômico.
III - Dois balões contendo 1 L de gás carbônico ou de hélio terão massas iguais destes gases, já que um mol de qualquer gás, nas condições ideais, ocupa 22,4 L.
(Dados: massa molar do
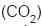 = 44 g/mol
= 44 g/mol massa molar do He = 4 g/mol
massa molar média do ar = 29 g/mol)
É(São) correta(s) APENAS a(s) afirmativa(s)