Questões de Concurso
Comentadas sobre sistemas heterogêneos: produto de solubilidade (kps). em química
Foram encontradas 26 questões
A partir das informações do texto precedente, julgue o próximo item.
Sais muito solúveis são aqueles que apresentam valores
elevados da constante do produto de solubilidade (Kps) em
uma dada temperatura.
Nessa temperatura, o valor da constante do produto de solubilidade desse sal é, aproximadamente,
Considere-se que, para a reação FeS (s) ⇌ Fe2+ (aq) + S2− (aq), a 25 °C, a constante do produto da solubilidade (Kps) seja igual a 2,56 × 10−18. Nesse caso, quando o equilíbrio for alcançado, a solubilidade do FeS em água será inferior a 2 × 10−7 g/L, desconsiderando-se qualquer hidrólise posterior dos íons.
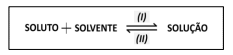
Resíduos de metais pesados gerados em laboratório químico podem ser tratados por reação de precipitação com carbonato, geralmente na forma de calcário. O sólido obtido é filtrado em papel e armazenado, sendo que o líquido filtrado é neutralizado antes do descarte. Para a separação de resíduos dos íons metálicos Pb2+ , Cd2+ e Cu2+, a precipitação ocorre de acordo com as seguintes reações:

Em relação às reações de precipitação e seus produtos de solubilidade (Kps), considere as afirmativas a seguir.
I - Cu2+ é o íon mais insolúvel da mistura na precipitação com íon 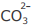
II - Pb2+ é o íon mais solúvel da mistura na precipitação com íon 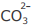
III - Cd2+ é mais insolúvel do que Cu2+ e Pb2+ na
precipitação com íon 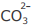
Está(ão) correta(s)
Na revelação de impressões digitais, uma das técnicas mais comuns envolve o uso de pós-reveladores como a ninidrina, o cianoacrilato e o nitrato de prata. Nesse último, o sal de prata reage com cloretos de secreções da pele, precipitando o cloreto de prata, sendo revelada com luz solar e fotografada rapidamente.
Sabendo que o produto de solubilidade desse sal é 1,8 x 10-10 mol/L, o composto a seguir que pode ser adicionado para recuperação da prata é o
Considere a mistura de 100 mL de sulfeto de sódio 0,2 mol L−1 com 100 mL de nitrato de chumbo 0,1 mol L−1 , resultando na formação do precipitado sulfeto de chumbo. A solubilidade, em mol L−1 , do sulfeto de chumbo na solução é de
(Dado: Kps PbS = 3,0x10−28)
Fe2O3 (s) + x H+ (aq) ⇌ y Fe3+ (aq) + z H2O (l)
Com base nessas informações, julgue o seguinte item.
A constante de equilíbrio K da reação do óxido de ferro (III) é corretamente expressa pela seguinte equação. K = [ Fe3+ ]y [ H20]z / [Fe2O3] [ H+]x
Julgue o item de quanto às reações e aos usos que envolvem o carbonato de cálcio e seus derivados.
Cavernas de calcário são formadas pela ação de dissolução das rochas calcárias pela água subterrânea, que contém dióxido de carbono, conforme a equação química a seguir.
CaCO2 (s) + H2O + CO (aq) --> Ca(HCO2)2 (aq)
A química ácido / base de muitos sistemas aquáticos naturais, incluindo rios e lagos, é dominada pela interação do íon carbonato, CO3 2-, uma base moderadamente forte, com ácido carbônico (H2 CO3 ), que é um ácido fraco. O ácido carbônico resulta da dissolução na água do gás carbônico e da decomposição da matéria orgânica na água. A fonte predominante de íon carbonato são as rochas calcárias, que são constituídas em grande medida por carbonato de cálcio (CaCO3 ). Embora esse sal seja quase insolúvel, uma pequena quantidade dele dissolve-se quando em contato com a água:
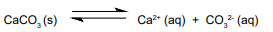
Considere que, em certa condição de temperatura do meio, a constante do produto de solubilidade (Kps) para o CaCO3 seja igual a 4 x 10–10. Nessas condições, qual é a massa de íon cálcio, em miligramas, dissolvida em 100 litros de solução?
Dado: massa atômica do cálcio = 40 u


Tendo como referência a figura e os dados da tabela precedentes, julgue o item a seguir.
Considere que a reação entre antimônio e sulfeto produza
o sal Sb2S3, pouco solúvel e de cor ocre que, em meio
aquoso, dissocia-se parcialmente, de acordo com o
equilíbrio Sb2S3(s)2Sb3+(aq) + 3S2-
(aq). Nesse caso,
a concentração de sulfeto necessária para iniciar a formação
do sólido Sb2S3 em uma solução aquosa de Sb3+
de concentração x mol/L deverá ser maior que
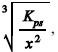 em que Kps é a constante de equilíbrio da reação precedente.
em que Kps é a constante de equilíbrio da reação precedente.
A adição de NH3(aq) a uma solução saturada de cloreto de prata em contato com o precipitado resultará
Considere uma solução aquosa 0,1 mol L−1 contendo os cátions Sr2+, Ca2+, Ba2+, Ra2+ e Pb2+.
Dadas as constantes do produto de solubilidade (KPS):
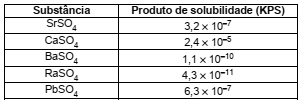
Se íons sulfato (SO2-4) forem gradualmente adicionados à solução acima,