Questões de Concurso
Comentadas sobre substâncias inorgânicas: dissociação iônica e ionização, conceitos de ácido-base. em química
Foram encontradas 72 questões
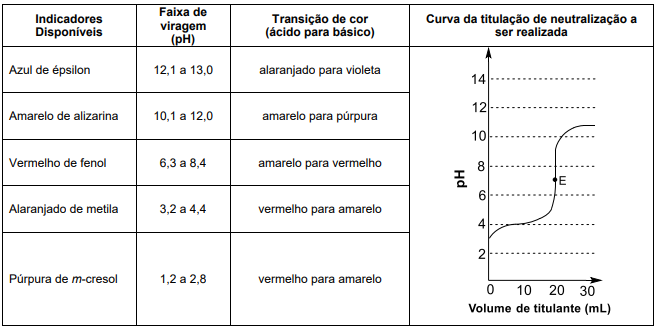
O indicador que o técnico deve utilizar é:
No tratamento de efluente por processos físico-químicos, são utilizados floculantes à base de Al2(SO4)3 ou FeCl3. A reação que produz a floculação ocorre em meio alcalino, de acordo com as reações descritas abaixo.
a Al2(SO4)3 + b NaOH c Al(OH)3 + d Na2SO4
e FeCl3 + f NaOH g Fe(OH)3 + h NaCl
Com relação às reações acima, pode-se afirmar que:
Um perito oficial dissolveu certa quantidade de um sal em solvente e, por alguma perturbação, parte do sal se depositou, produzindo uma solução. Pode-se considerar nominalmente essa solução como:
A utilização de histórias em quadrinhos para auxiliar o processo de ensino-aprendizagem vem crescendo nos últimos anos, especialmente, nas disciplinas de ciências exatas e da terra. A figura abaixo foi extraída da revista em quadrinhos HQUÍMICA:
Estequionópolis, Cruz Filho et al, 2016, FUESPI, Teresina-PI, que aborda os assuntos de funções inorgânicas, reações químicas e estequiometria, dentre outros, em uma trama que envolve a investigação do assassinato de um pesquisador.
No trecho em destaque, cena do crime, o investigador vê evidências de metais "corroídos" por ácidos e destaca a presença de alguns deles. Quais dos ácidos citados é poliprótico, forte e pode ter reagido com os metais na cena do crime?
Os valores de energia de ionização para um átomo informam a respeito da sua distribuição eletrônica.
Em relação ao gráfico anterior, analise as afirmativas.
I. O aumento nos valores de energia de ionização correspondente à remoção dos cinco primeiros elétrons ocorre em função do aumento da carga nuclear efetiva.
II. Os cinco primeiros elétrons removidos se encontram no mesmo subnível.
III. O grande incremento no valor da energia de ionização referente ao sexto elétron é um indicativo que este se encontra em um nível de energia mais próximo do núcleo que o quinto elétron.
IV. O elemento químico em questão pertence à coluna 17 da tabela periódica.
Estão corretas apenas as afirmativas
Analise a imagem abaixo e responda
Fonte : BROWN, Theodore; LEMAY, H. Eugene;
BURSTEN, Bruce E. Química: a ciência central. 9ª
ed. Prentice-Hall, 2005. (adaptado)
A imagem acima mostra uma:
Qual das seguintes alternativas descreve corretamente a diferença entre os conceitos de ácidos e bases de Brønsted-Lowry e de Lewis?
A função inorgânica ácido é fundamental na química, sendo caracterizada pela capacidade de doar prótons em solução aquosa. Os ácidos são amplamente utilizados em diversos contextos, desde aplicações industriais até processos biológicos. Em termos de nomenclatura, compreender seus diferentes nomes é essencial para identificar corretamente essas substâncias na prática química.
Entre os ácidos: HClO3, HClO2, HClO4 e HClO, assinale a alternativa CORRETA que corresponde a nomenclatura de cada ácido, respectivamente.
A compreensão dos conceitos de ácidos e bases é fundamental para a química e tem sido moldada por diferentes teorias ao longo do tempo. A teoria de Arrhenius, proposta no final do século XIX, define ácidos como substâncias que liberam íons de hidrogênio (H+) em solução aquosa e bases como substâncias que liberam íons hidroxila (OH-) em solução aquosa. Em contrapartida a teoria de Bronsted-Lowry, desenvolvida em 1923, ampliou essa definição ao considerar ácidos como doadores de prótons e bases como receptores de prótons, independente da presença de água. Ambas as teorias são fundamentais para o entendimento das propriedades ácido-base e são aplicadas em diversos campos da química.
A seguir, observe as reações:
Em relação a Teoria de Bronsted-Lowry e as reações dadas anteriormente, julgue as afirmativas abaixo como V para verdadeiro e F para falso.
( ) Nas reações I, III e IV o NH+ 4, H2O e HSO-4, respectivamente, são ácidos.
( ) Ambas as reações II e III possuem o mesmo ácido, mas com base conjugada diferente.
( ) A reação V apresenta H3O+ como ácido e HSO-3 como base.
( ) A reação I tem como ácido CN- , ácido conjugado o HCN e a base conjugada NH3.
( ) Dentre as cinco reações, há uma entre elas com o OH- como sendo seu ácido conjugado.
Qual das seguintes alternativas apresenta a sequência CORRETA?
Um técnico necessita preparar uma solução contendo ácido clorídrico e ácido acético em mistura, com concentrações de 0,05 mol/L e 0,06 mol/L, respectivamente.
No laboratório, ele dispõe de água destilada e um balão volumétrico de 500 mL, além das demais vidrarias necessárias. No almoxarifado, ele dispõe de soluções cujos rótulos estão representados abaixo.
Dados:
Massa molar do ácido clorídrico: 36,5 g/mol
Massa molar do ácido acético: 60 g/mol
Qual das opções a seguir apresenta os volumes corretos de cada ácido que o técnico deve usar para que obtenha a solução de que precisa?
Acerca de eletrodos de membrana de vidro, titulação potenciométrica e medida de condutividade, julgue o item subsequente.
A condutividade elétrica é uma propriedade que depende da
presença de íons dissolvidos em soluções iônicas, como
ácidos, bases e sais, pois os íons permitem a passagem da
corrente elétrica. A medida da condutividade é afetada pela
temperatura, geralmente decrescendo com o aumento da
temperatura.
• 500 mL de solução de fluoreto de magnésio com concentração 0,020 mol L-1
• 200 mL de solução de fluoreto de alumínio com concentração 3,36 g L-1
• 300 mL de solução de fluoreto de sódio com concentração 0,060 mol L-1
Admitindo-se que os solutos estão completamente dissociados, a concentração de íons fluoreto, em mol L-1 , na solução resultante da mistura é igual a
Dado
Al = 27 g mol-1 F = 19 g mol-1
6 Fe2+ (aq) + Cr2 O7 2+ (aq) + 14 H+ → 6 Fe3+ (aq) + 2 Cr3+ (aq) + 7 H2 O(l)
Com base nessas informações, a quantidade, em mol, de Fe2+ na solução de amostra é
[Ni(NH3)6]SO4; [CoCl2(NH3)4]Cl; K4[Fe(CN)6]; [Mn(CN)6]4-; [Fe(Cl)4]2-; [Co(Cl)3(NH3)3]
(i) um ácido forte for adicionado?
(ii) uma base forte for adicionada?
4 Au(minério) + 8 NaCN(aq) + O2(g) + 2 H2O(l) → 4 Na[Au(CN)2](aq) + 4 NaOH(aq)
A espécie química solúvel [Au(CN)2]− é posteriormente imobilizada sobre carvão ativado, e o ouro é recuperado por redução eletroquímica:
[Au(CN)2]−(aq) + e− → Au(s) + 2 CN−(aq)
Dados: Massa molar (g mol−1): Au = 197, NaCN = 49.
Considerando a estequiometria das reações, qual é a massa de ouro que se espera extrair, utilizando-se 1 kg de cianeto de sódio?
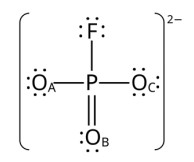
Ao se calcular as cargas formais de cada átomo na estrutura apresentada, conclui-se que são nulas, com exceção dos átomos:
Coluna 1 Substâncias Inorgânicas
1. Al2(SO4)3 2. HNO3 3. NaClO 4. H2CO3 5. BaSO4
Coluna 2 Aplicações
( ) Em água mineral gaseificada ( ) Como desinfetante e alvejante ( ) No tratamento de águas ( ) Contraste em radiografias ( ) Na fabricação de fertilizantes e explosivos
Assinale a alternativa que indica a sequência correta, de cima para baixo.