Questões de Concurso Público SEEDUC-RJ 2013 para Professor - Química
Foram encontradas 20 questões
(Adaptado de: Revista Pesquisa FAPESP n. 198. Disponível em: http://agencia. fapesp.br/16030. Acesso em janeiro de 2013.)
O óxido citado no texto pode ser classificado como:
Cientistas conseguiram realizar um experimento pelo qual demonstraram que o núcleo atômico pode se tornar transparente.(...)
A técnica, que utiliza o efeito da transparência induzida eletromagneticamente, permite que materiais opacos possam se tornar transparentes à luz em certos comprimentos de onda, como o raio X (...). Esse efeito é promovido pela interação complexa da luz com a eletrosfera, onde estão os elétrons.
Esse trabalho demonstrou que o efeito também existe quando raio X é direcionado para o núcleo atômico do isótopo de ferro 57, que compreende 2% do ferro que ocorre naturalmente no planeta.
(Adaptado de: http://agencia.fapesp.br/15156. Acesso em fevereiro de 2013.)
A estrutura atômica desse isótopo do ferro apresenta:
CCl3 CHCl2 (g) + 2 HF(g) → CCl 3 CHF2 (g) + 2 HCl(g)
Utilizando as energias de ligação médias:
Ligação Energia de Ligação (kJ.mol–1)
C–Cl 338
C–F 484
H–F 565
H–Cl 431
A variação de entalpia da reação apresentada, em kJ.mol–1 , é igual a:
Considere a ocorrência dessa reação em um sistema no qual o equilíbrio será alcançado. Segundo o princípio de Le Chatelier, um fator que pode deslocar esse equilíbrio no sentido da diminuição da concentração de dióxido de enxofre é:
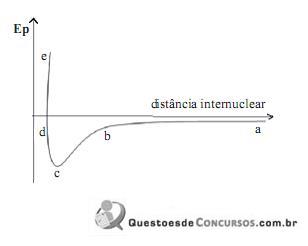
O ponto da curva relacionado com o comprimento da ligação química está representado pela letra:
Relacionando as posições dos elementos citados na classificação periódica com suas propriedades, é correto afirmar que:
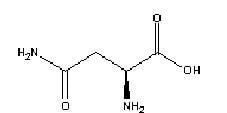
Uma propriedade física que pode ser utilizada para diferenciar os isômeros espaciais dessa substância é:
O número de moléculas dessa toxina que corresponde à dose citada corresponde, aproximadamente, a:
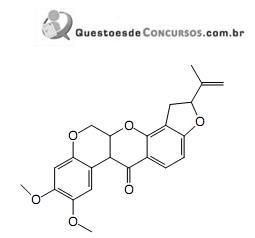
As funções orgânicas presentes na estrutura da rotenona são:
Dado: log 0,625 = – 0,2
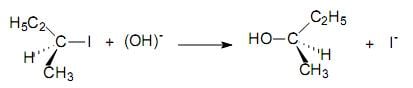
O diagrama de energia potencial indica que essa reação ocorre em uma etapa e pode ser esquematizado como:
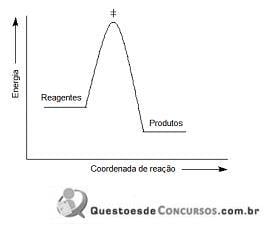
Analisando a equação química e o diagrama de energia esquematizado, a reação apresentada pode ser classificada como uma:
Mg2 SiO4 + 4HCl → 2MgCl 2 + 2H2 O + SiO2
MgCl 2 + H2 CO3 → MgCO3 + 2HCl
Nesse processo, a quantidade de silicato de magnésio (em toneladas) necessária para reagir completamente com 6,2 toneladas de ácido carbônico é igual a:
(STRATHERN, P. O sonho de Mendeleiev, 1ª edição. Rio de Janeiro, RJ: Jorge Zahar Editor, 2002, p.219.)
Na reação realizada por Wöhler ocorreu uma:
(Disponível em: http://oglobo.globo.com/ciencia/eua-voltam-produzir-plutonio-para- alimentar-sondas-espaciais-7881294. Acesso em março de 2013.)
Este radionuclídeo pode ser sintetizado pelo bombardeio de núcleos de urânio-238 com deutério, produzindo netúnio-238. O netúnio-238 sofre um decaimento produzindo o plutônio-238, esse decaimento ocorre com a emissão de partícula: