Questões de Concurso Público Petrobras 2011 para Químico de Petróleo Júnior
Foram encontradas 31 questões
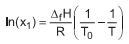
Sabe-se que:
• X1 é a fração molar de solvente em solução que cristaliza na temperatura T;
• ΔfH e T0 são, respectivamente, a variação de entalpia e a temperatura de fusão do solvente puro;
• R é a constante universal dos gases que pode ser aproximada por 2 cal/(mol•K);
• a variação de entropia de fusão do benzeno puro é 8 cal/(mol•K);
• a massa molar do benzeno é 78 g/mol;
• a temperatura de fusão do benzeno (T0) é 278,5 K.
A massa molar do soluto, a 278 K, necessária para a cristalização do benzeno a partir de uma solução de 10 g de soluto em 780 g de benzeno, em g/mol, é
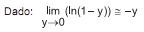
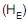 e a energia interna específica do gás no interior do tanque, após o enchimento (U), é
e a energia interna específica do gás no interior do tanque, após o enchimento (U), é1. de um estado inicial a 100 o C e 1 bar, é comprimido adiabaticamente até 150 o C;
2. em seguida, é resfriado de 150 o C a 100 o C, a pressão constante;
3. finalmente, é expandido isotermicamente até o seu estado original.
Para o ciclo completo, as variações de energia interna (?U) e entalpia (?H) são
 U + PV e G
U + PV e G H - TS, em que:
H - TS, em que:H = entalpia molar;
G = energia livre de Gibbs molar;
S = entropia molar;
P = pressão;
T = temperatura;
V = volume molar,
para este processo de compressão, conclui-se que
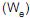 como trabalho de eixo, a equação que expressa a primeira lei da termodinâmica para um processo com escoamento, em estado estacionário, entre uma única entrada e uma única saída, em que as variações de energia cinética e potencial são desprezíveis, é
como trabalho de eixo, a equação que expressa a primeira lei da termodinâmica para um processo com escoamento, em estado estacionário, entre uma única entrada e uma única saída, em que as variações de energia cinética e potencial são desprezíveis, é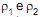 , sendo
, sendo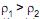 . Se 70% do volume da esfera está submerso no líquido mais denso, a massa específica da esfera é
. Se 70% do volume da esfera está submerso no líquido mais denso, a massa específica da esfera é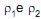 . O cubo flutua na configuração mais estável e em repouso na superfície livre de um líquido com massa es- pecífica ?3 em equilíbrio estático. Acima do líquido existe ar cujos efeitos podem ser desprezados. Sabendo-se que
. O cubo flutua na configuração mais estável e em repouso na superfície livre de um líquido com massa es- pecífica ?3 em equilíbrio estático. Acima do líquido existe ar cujos efeitos podem ser desprezados. Sabendo-se que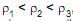 , e que o centro geométrico do cubo está situado a uma distância Z abaixo da interface líquido – ar, o valor de Z é
, e que o centro geométrico do cubo está situado a uma distância Z abaixo da interface líquido – ar, o valor de Z ém fluido newtoniano incompressível, com massa específica ρ, escoa com vazão mássica W em uma tubulação de diâmetro D e comprimento equivalente L, num local onde a aceleração da gravidade é g. Se o fator de atrito é f, a perda de carga (energia por unidade de peso de fluido) associada é
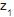 = -5 m até a cota
= -5 m até a cota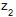 = 10 m, onde a pressão é atmosférica. Se a perda de carga associada ao escoamento é de 3 m de coluna do referido fluido, a pressão manométrica na tubulação na cota
= 10 m, onde a pressão é atmosférica. Se a perda de carga associada ao escoamento é de 3 m de coluna do referido fluido, a pressão manométrica na tubulação na cota 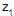 é
é• um reservatório quente (fonte quente), onde o fluído absorve uma quantidade de calor
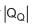 ;
; • um reservatório frio (fonte fria), onde o fluido descarta uma quantidade de calor
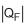 .
. Se a quantidade de trabalho líquido produzida por esse fluído for igual a
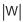 , então a eficiência térmica
, então a eficiência térmica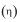 dessa máquina é dada por
dessa máquina é dada por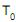 e a uma pressão
e a uma pressão 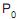 , até um estado final a uma temperatura T e a uma pressão P. Se
, até um estado final a uma temperatura T e a uma pressão P. Se 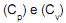 são as capacidades caloríficas molares deste gás, a pressão e volume constantes, respectivamente, e se R é a constante universal dos gases, a expressão para o cálculo da variação de entropia (?S) desse processo é
são as capacidades caloríficas molares deste gás, a pressão e volume constantes, respectivamente, e se R é a constante universal dos gases, a expressão para o cálculo da variação de entropia (?S) desse processo é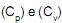 como as capacidades caloríficas molares, de um gás ideal, a pressão constante e volume constante, respectivamente, e (?) como a razão entre estas capacidades caloríficas
como as capacidades caloríficas molares, de um gás ideal, a pressão constante e volume constante, respectivamente, e (?) como a razão entre estas capacidades caloríficas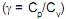 . A equação que relaciona a pressão e o volume de um gás ideal em um processo adiabático reversível, quando estas capacidades caloríficas são constantes, é dada por
. A equação que relaciona a pressão e o volume de um gás ideal em um processo adiabático reversível, quando estas capacidades caloríficas são constantes, é dada por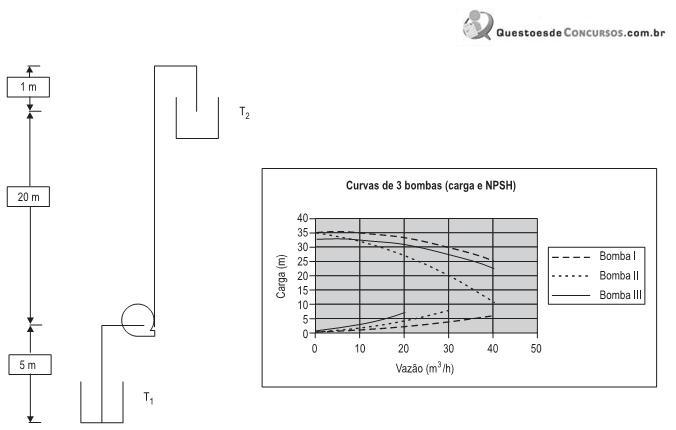
O esquema acima representa um arranjo para transferência de uma solução aquosa (? = 1.000 kg/m3 ) de um tanque
 para outro
para outro , ambos a pressão atmosférica. A vazão necessária é de 20 m3 /h e, nessas condições, a perda de carga por atrito na tubulação é igual a 20% da carga de elevação. Com base nesses dados, pode(m) ser utilizada(s) a(s) bomba(s)
, ambos a pressão atmosférica. A vazão necessária é de 20 m3 /h e, nessas condições, a perda de carga por atrito na tubulação é igual a 20% da carga de elevação. Com base nesses dados, pode(m) ser utilizada(s) a(s) bomba(s)I - Um fluido cuja viscosidade aumenta com a taxa de cisalhamento é chamado de pseudoplástico.
II - Se a viscosidade de um fluido for constante em certa faixa de taxa de cisalhamento, ele sempre se comportará como newtoniano para outras faixas de taxa cisalhante.
III - Existem fluidos que necessitam de uma tensão crítica para começar a escoar e, uma vez superada essa tensão crítica, ele escoa obedecendo ao modelo de Newton.
IV - Certos fluidos apresentam uma viscosidade constante para faixas de valores baixos e altos da taxa cisalhante e uma viscosidade decrescente para uma faixa intermediária de taxa de cisalhamento.
V - Fluidos tixotrópicos são aqueles que apresentam uma redução na viscosidade à medida que a taxa de cisalhamento aumenta.
Está correto APENAS o que se afirma em
I - A filtração ocorre no regime permanente.
II - A vazão cresce continuamente durante a filtração.
III - É possível eliminar-se a colmatação da torta com a adição de um auxiliar de filtração à suspensão a ser filtrada.
IV - Nas filtrações que requerem auxiliar de filtração, o auxiliar mais comumente empregado é a terra diatomácea, também conhecida como diatomita ou Kieselguhr.
São corretas APENAS as afirmativas
I - Aumento na vazão alimentada ao hidrociclone.
II - Aumento da queda de pressão de operação.
III - Aumento da concentração de cascalhos na suspensão alimentada ao hidrociclone.
IV - Aumento na viscosidade da suspensão alimentada ao hidrociclone.
São corretos APENAS os fatores