Questões de Concurso Público Innova 2012 para Técnico de Operação Júnior
Foram encontradas 50 questões
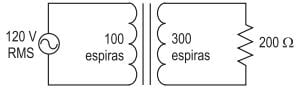
O enrolamento primário do transformador possui 100 espiras, e o secundário possui 300 espiras.
Qual é, aproximadamente, o valor RMS da intensidade da corrente que atravessa o resistor?
Listando-se as radiações eletromagnéticas em ordem crescente de frequência, tem-se
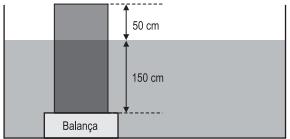
O valor, em N, indicado pela balança é aproximadamente igual a
Dados Densidade do paralelepípedo = 1,8 x 103 kg/m3 Densidade da água = 1,0 x 103 kg/m3 Aceleração da gravidade = 10 m/s2
Se a lancha e o helicóptero partem simultaneamente, qual é aproximadamente o intervalo de tempo, em minutos, entre a chegada do helicóptero e da lancha à plataforma?
S(s) + ½ O2(g) → SO(g)
SO(g) + ½ O2(g) → SO2(g)
SO2(g) + ½ O2(g) → SO3(g)
SO3(g) + H2O(l) → H2SO4(aq)
Considerando rendimento de 80% na formação de ácido sulfúrico a partir do S, a massa, em g, do ácido produzida a partir de 50,0 g da amostra original é, aproximadamente,
KMnO4(aq) + SnSO4(aq) + H2SO4(aq) → MnSO4(aq) + Sn(SO4)2(aq) + K2SO4(aq) + H2O( l)
Considere as afirmações abaixo sobre essa reação.
I - MnO4 - é o agente oxidante no meio ácido, e Sn2+ , o agente redutor.
II - No balanço de massa, 2 mol de KMnO4 reagem com 5 mol de SnSO4 .
III - Sn2+ ganha 2 elétrons do MnO4 - ao passar para Sn4+ .
É correto APENAS o que se afirma em
Em meio aquoso, ele se ioniza de acordo com a equação simplificada (I) abaixo.
(I) HC2H3O2(aq)
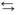 H+(aq) + C2H3O2−(aq)
H+(aq) + C2H3O2−(aq) Ácido clorídrico é um ácido muito forte e, em meio aquoso, ele se ioniza de acordo com a equação simplificada (II) abaixo.
(II) HCl(aq) → H+(aq) + Cl−(aq)
Na reação da base forte hidróxido de sódio 0,1 mol/L com o ácido etanoico 0,1 mol/L, e com o ácido forte
 0,1 mol/L, ambos em meio aquoso, ocorrem as seguintes reações:
0,1 mol/L, ambos em meio aquoso, ocorrem as seguintes reações: (III) NaOH(aq) + HC2H3O2(aq) → NaC2H3O2(aq) + H2O(l)
(IV) NaOH(aq) + HCl(aq) → NaCl(aq) + H2O(l)
Sobre a ionização em (I) e (II) e as reações de neutralização em (III) e (IV), tem-se que: