Questões de Concurso Público Petrobras 2014 para Técnico(a) Químico(a) de Petróleo Junior
Foram encontradas 39 questões
2NaOH(aq) + H2 SO4(aq) → 2H2 O(l) + Na2 SO4(aq)
Nesse experimento, a massa, em gramas, de NaOH que reage por completo com 2,94 g de H2 SO4 é
Mg(s)+ 2HCl(aq) → MgCl2(aq) + H 2(g)
A quantidade máxima de H2 obtida no experimento, em miligrama, considerando comportamento de gás ideal, é, aproximadamente, igual a:
Dados:
constante dos gases = 62,3 mmHg L K-1 mol -1
Admitindo comportamento de gases ideais, se 140 g é a quantidade máxima de gás nitrogênio (N2 ) que pode ser introduzida no primeiro cilindro, a quantidade máxima de gás metano (CH4 ), em gramas, que pode ser introduzida no segundo cilindro é
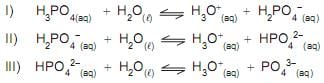
De acordo com o conceito ácido-base de Bronsted e Lowry, na equação

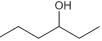
O produto orgânico desta oxidação é
Na cromatografia em camada fina, o(a)
A expressão para se obter o valor de k é
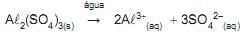
Um técnico pesou, em balança semianalítica, 17,1 g de Al2 (SO4 ) 3 , dissolveu o sal em água e levou o volume da solução a 500 mL em balão volumétrico.
As concentrações de Al3+ e SO42- , em mol/L, após a dissolução naquele volume final são, respectivamente,
A concentração de KIO3 na solução preparada em quantidade de matéria, em mol L-1 , é
Dado
M (KIO3 ) = 214 g mol -1
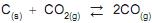
Para esse equilíbrio, a expressão da constante de equilíbrio Kc em função das concentrações das espécies, em quantidade de matéria, é:
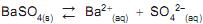
Sendo o seu produto de solubilidade a 25 o C igual a 1,0 x 10-10 , em solução saturada, a concentração de Ba 2+ , em mol/L, é

Um indicador do ponto final da titulação apropriado para uso nessa análise é o(a)
Uma amostra sólida contendo bário é solubilizada e, a seguir, precipitada com sulfato formando o precipitado de BaSO4. Essa reação está representada a seguir.
Ba2+ (aq)+ SO42- (aq) → BaSO4(s)
Para uma amostra sólida pesando 1,000 g houve formação de 0,932 g BaSO4 (reação completa). A porcentagem em massa de bário na amostra sólida é, aproximadamente, igual a
NÃO é pertinente a esse método a(o)

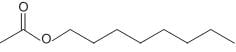
A substância representada na Figura acima é um flavorizante obtido sinteticamente (a partir de um ácido carboxílico e um álcool) utilizado em diversos alimentos e bebidas.
De acordo com as regras da IUPAC, sua nomenclatura é
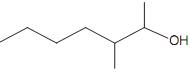
A função orgânica oxigenada e a nomenclatura de acordo com as regras da IUPAC dessa substância são, respectivamente,