Questões de Concurso Público Petrobras 2014 para Técnico de Inspeção de Equipamentos e Instalações Júnior
Foram encontradas 14 questões
Considerando o valor da constante de Faraday igual a 96.500 C, e que essa é a quantidade de carga elétrica de 1 mol de elétrons, qual é a quantidade máxima, em gramas, de sódio metálico que se forma, com a carga elétrica de 386.000 C, na eletrólise ígnea do NaCl?
Dado
M(Na) = 23 g/mol

Utilize as informações contidas na Tabela de potenciais de redução abaixo para responder a questão.
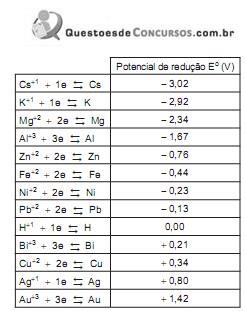
Considere a pilha abaixo representada pela seguinte equação:
Com o exclusivo objetivo de neutralizar o ácido, o procedimento correto deve ser o de jogar no asfalto solução aquosa de
Com respeito a essa propriedade, o(a)

Na reação de oxirredução representada pela equação não balanceada acima, o número de oxidação médio do.
Esse fenômeno é denominado
H2 + 1/2 O2 → H2O
Nesse processo, quantos mols de O2 são necessários para produzir 10 mols de H2 O?
Qual é, em J, a energia retirada para congelar os 100 g de água?
Dados
Lfusão = 336 J/g
cágua = 4,2 J/g.° C

I - É função do revestimento impedir a mistura do material da alma metálica com o metal de solda.
II - É função do revestimento a remoção dos elementos de liga do metal de solda.
III - É função do revestimento o isolamento mecânico da alma metálica.
É correto APENAS o que se afirma em
A energia necessária para levar o gelo até a temperatura de fusão e a energia necessária para fundir o gelo, são, em J, respectivamente,
Considere
cgelo = 2,2 J/g K
LF =330 J/g
2 Ca3 Si O5 + X H2O → ( 3 CaO . 2 Si O2 . 4 H2 O ) + Y Ca( OH)2 + 173,6 kJ
Os coeficientes estequiométricos X e Y são, respectivamente,