Questões de Concurso Público Transpetro 2023 para Técnico Químico de Petróleo
Foram encontradas 60 questões
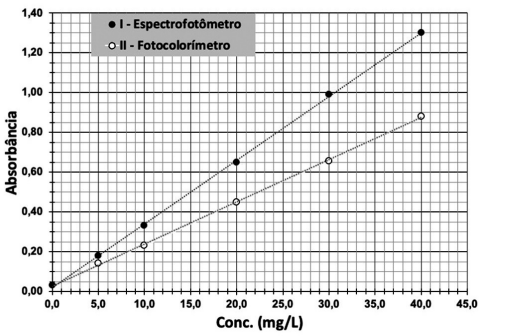
Admita que uma amostra desconhecida do mesmo analito, denominada solução A, foi diluída duas vezes, formando a solução B. A absorbância da solução B foi de 0,60 nas mesmas condições da curva de calibração com maior sensibilidade apresentada na Figura acima.
A concentração do analito na amostra desconhecida antes de diluição (solução A), em mg L-1 , era de
LOD = 3 x (desvio padrão do branco / inclinação da curva de calibração) LOQ = 10 x (desvio padrão do branco / inclinação da curva de calibração)
Considere que um procedimento de validação foi feito para determinar o LOD e o LOQ de um certo método analítico em espectroscopia de absorção atômica. Foram feitas dez medições do branco que, por sua vez, produziram valor médio = 4,24 x 10-3 com desvio padrão = 3,42 x 10-4 . A equação da reta da curva de calibração do método, com os seus respectivos coeficientes angular e linear, foi:
Absorbância = 3,42 x 10-3 conc. (mg L-1 ) + 2,23 x 10-3
O coeficiente de determinação (R2 ) da curva de calibração foi 0,9994. Com base nesses dados, os valores de LOD e de LOQ, em mg L-1 , foram, respectivamente,
Em relação à técnica de cromatografia, o termo partição significa
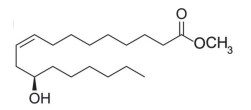
De acordo com as regras de nomenclatura da IUPAC, o nome do ricinoleato de metila é
A massa, em gramas, de soluto a ser empregada no preparo dessa solução corresponde a
Dado massas molares: Ca = 40 g mol-1 Br = 80 g mol-1
A fórmula química desse sal é
A fórmula molecular desse ácido é
A geometria molecular da fosfina é nomeada
Nessa eletrólise, a substância simples formada no catodo é
Admitindo-se que há completa dissociação dos solutos, a concentração de íons K+ , em mol L-1 , na solução formada é igual a
Sabendo-se que a pressão no recipiente é de 1,2 atm e que o gás apresenta comportamento ideal, a massa de etano, em gramas, presente no interior do recipiente é igual a
Dado
constante dos gases ideais: 0,08 atm L mol-1 K-1
massas molares: C = 12 g mol-1, H = 1 g mol-1
H2 (g) + I2 (g) ⇌ 2 HI (g)
Em um reator, as concentrações iniciais de H2 e I2 foram respectivamente iguais a 3,0 mol L-1 e a 3,5 mol L-1 . Atingido o equilíbrio, a concentração de HI foi de 5 mol L-1 . Nas condições do reator, a constante de equilíbrio da reação em termos de concentrações é igual a
Admitindo-se comportamento ideal para esses gases, a pressão parcial do metano, em atm, é, aproximadamente,
Dado
constante dos gases ideais = 0,08 atm L mol-1 K-1
CaCO3 (s) + 2 HCl(aq) → CaCl2 (aq) + H2 O(l) + CO2 (g)
Nessa análise, as impurezas presentes não reagiram e houve o completo consumo do carbonato de cálcio, com formação de 0,66 g de CO2 .
O grau de pureza do carbonato de cálcio na amostra é igual a
Dado
massas molares: Ca = 40 g mol-1,
C = 12 g mol-1, H = 1 g mol-1,
O = 16 g mol-1, Cl = 35,5 g mol-1
Nesse processo, a massa de eteno, em quilogramas, necessária para produzir 8.720 kg de bromoetano é igual a
Dado massas molares: C = 12 g mol-1 , H = 1 g mol-1, Br = 80 g mol-1
A concentração, em g L-1 , de hidróxido de potássio na solução comercial correspondeu a, aproximadamente,
Dado massas molares: K = 39 g mol-1, H = 1 g mol-1, O = 16 g mol-1
A dimetilglioxima é um reagente específico na análise gravimétrica.
Esse reagente é empregado para a determinação do cátion
Em uma síntese industrial, o HBr é produzido a partir da seguinte reação química:
H2 (g) + Br2 (g) → 2 HBr (g)
No início da síntese, a concentração de H2
era de 0,3 mol/L.
Após 20 minutos, sua concentração passou a 0,1 mol/L.
Nesse intervalo de tempo, a velocidade média de formação de HBr, em mol L-1
min-1
, correspondeu a
Em um experimento, realizou-se um estudo cinético da seguinte reação química:
2 N2 O5 (g) → 4 NO2 (g) + O2 (g)
Esse estudo indicou que essa é uma reação química de
primeira ordem e que a constante de velocidade é igual
a 3,4 x 10-4 s-1 a 25ºC.
Para uma concentração de N2
O5
igual a 0,2 mol L-1
, a
velocidade da reação, em mol L-1
s-1
, corresponde a