Questões de Concurso Público FUB 2009 para Químico
Foram encontradas 50 questões

O tempo morto, ou seja, o tempo médio necessário para que uma molécula da fase móvel passe através da coluna, foi de 2 min. A calibração foi realizada analisando-se uma mistura-padrão de A e B e utilizando-se o método da normalização da área, cujos dados são apresentados na tabela a seguir.

Considerando as informações fornecidas, julgue os itens subsequentes.
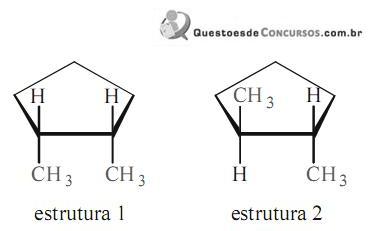
Acerca das estruturas apresentadas acima, julgue o itens.
As estruturas 1 e 2 representam diferentes conformações de um mesmo composto.

A reação do brometo de alquila com um íon alcóxido pode levar à formação de um alceno ou de um éter, conforme representado na figura acima.
Acerca dessas reações, julgue os itens.

A reação do brometo de alquila com um íon alcóxido pode levar à formação de um alceno ou de um éter, conforme representado na figura acima.
Acerca dessas reações, julgue os itens.

Alcoois podem ser formados a partir da reação de hidratação de alcenos catalisada por ácido. Um exemplo é a hidratação do 3,3-dimetil-1-buteno, mostrada acima.
Com relação a essa reação, julgue os itens.

Alcoois podem ser formados a partir da reação de hidratação de alcenos catalisada por ácido. Um exemplo é a hidratação do 3,3-dimetil-1-buteno, mostrada acima.
Com relação a essa reação, julgue os itens.

Acerca dos quatro compostos acima apresentados, julgue os itens.

Acerca dos quatro compostos acima apresentados, julgue os itens.

Acerca dos quatro compostos acima apresentados, julgue os itens.

Considerando as estruturas apresentadas acima, que correspondem a dois aldeídos e dois ácidos carboxílicos de grande ocorrência natural, julgue os itens subsequentes.

Considerando as estruturas apresentadas acima, que correspondem a dois aldeídos e dois ácidos carboxílicos de grande ocorrência natural, julgue os itens subsequentes.

Considerando as estruturas apresentadas acima, que correspondem a dois aldeídos e dois ácidos carboxílicos de grande ocorrência natural, julgue os itens subsequentes.

Considerando as estruturas apresentadas acima, que correspondem a dois aldeídos e dois ácidos carboxílicos de grande ocorrência natural, julgue os itens subsequentes.

Considerando as estruturas apresentadas acima, que correspondem a dois aldeídos e dois ácidos carboxílicos de grande ocorrência natural, julgue os itens subsequentes.
Com relação a esse assunto, julgue os itens.
Com relação a esse assunto, julgue os itens.
Com relação a esse assunto, julgue os itens.
A respeito da classificação das substâncias e suas características, julgue os itens.
A respeito da classificação das substâncias e suas características, julgue os itens.
A respeito da classificação das substâncias e suas características, julgue os itens.