Questões de Concurso Público PC-RR 2003 para Perito Criminal
Foram encontradas 19 questões
A presença da metanfetamina — uma droga alucinógena ilícita — em fluidos biológicos pode ser determinada por espectrometria de massa. O espectro de massa da metanfetamina apresenta um pico de 58 u bastante característico. A partir da fórmula estrutural da metanfetamina mostrada acima e considerando que M(H) = 1 g/mol, M(C) = 12 g/mol e M(N) = 14 g/mol, julgue o item a seguir.
O pico de 58 u deve-se ao fragmento CH3CH=NH+ CH3, que pode ser formado pelo seguinte mecanismo.
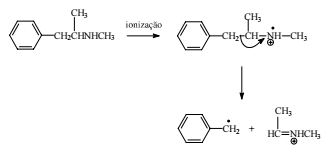
A presença da metanfetamina — uma droga alucinógena ilícita — em fluidos biológicos pode ser determinada por espectrometria de massa. O espectro de massa da metanfetamina apresenta um pico de 58 u bastante característico. A partir da fórmula estrutural da metanfetamina mostrada acima e considerando que M(H) = 1 g/mol, M(C) = 12 g/mol e M(N) = 14 g/mol, julgue o item a seguir.
Se o espectrômetro de massa utilizado tiver resolução igual a 2.000,
ele será capaz de separar um fragmento iônico de massa 499,9 u de
um fragmento iônico de massa 500,0 u.
A presença da metanfetamina — uma droga alucinógena ilícita — em fluidos biológicos pode ser determinada por espectrometria de massa. O espectro de massa da metanfetamina apresenta um pico de 58 u bastante característico. A partir da fórmula estrutural da metanfetamina mostrada acima e considerando que M(H) = 1 g/mol, M(C) = 12 g/mol e M(N) = 14 g/mol, julgue o item a seguir.
Se a metanfetamina for agitada na presença de cloreto de
benzenosulfonila em solução aquosa alcalina a frio, o resultado será
um material homogêneo.
A presença da metanfetamina — uma droga alucinógena ilícita — em fluidos biológicos pode ser determinada por espectrometria de massa. O espectro de massa da metanfetamina apresenta um pico de 58 u bastante característico. A partir da fórmula estrutural da metanfetamina mostrada acima e considerando que M(H) = 1 g/mol, M(C) = 12 g/mol e M(N) = 14 g/mol, julgue o item a seguir.
Existem dois enanciômeros da metanfetamina capazes de desviar o
plano da luz polarizada.
A presença da metanfetamina — uma droga alucinógena ilícita — em fluidos biológicos pode ser determinada por espectrometria de massa. O espectro de massa da metanfetamina apresenta um pico de 58 u bastante característico. A partir da fórmula estrutural da metanfetamina mostrada acima e considerando que M(H) = 1 g/mol, M(C) = 12 g/mol e M(N) = 14 g/mol, julgue o item a seguir.
Admita que o advogado de um réu acusado de ter consumido metanfetamina tenha proferido em sua defesa a seguinte frase.
“Não existe substância tóxica, mas sim doses tóxicas.”
Do ponto de vista estritamente químico, a frase do advogado pode
ser considerada correta, pois existe uma concentração abaixo da qual
a metanfetamina não causa nenhum efeito nocivo ao organismo,
assim como existe uma concentração acima da qual até cloreto de
sódio pode levar um indivíduo à morte.
Considere a seguinte situação hipotética.
Uma enfermeira é suspeita de ter trocado deliberadamente o conteúdo de um frasco de remédio, retirando a droga nele contida e substituindo-a por solução salina. Um agente policial submeteu o frasco em questão, que continha no rótulo a informação “meperidina 20 mg/mL”, a análise forense. O químico pipetou 100 μL da solução contida no frasco e a diluiu em H2SO4 0,5 mol/L até atingir o volume de 10,0 mL. Após agitar a solução, essa foi colocada em uma cubeta de 1 cm e um espectro de UV-VIS foi registrado. O químico observou que o espectro obtido era qualitativamente similar ao espectro de referência da meperidina e que a absorvância a 257 nm era igual a 0,075.
Nessa situação, sabendo-se que a absortividade molar da meperidina a 257 nm é igual a 0,85 L × g-1 × cm-1 em solução ácida e que a sua massa molar é igual a 247,3 g/mol, julgue o item subseqüente.
Admitindo-se que a informação contida no rótulo do frasco esteja
correta, após a diluição realizada pelo químico a concentração final de
meperidina será igual a 2,0 mg/mL.
Considere a seguinte situação hipotética.
Uma enfermeira é suspeita de ter trocado deliberadamente o conteúdo de um frasco de remédio, retirando a droga nele contida e substituindo-a por solução salina. Um agente policial submeteu o frasco em questão, que continha no rótulo a informação “meperidina 20 mg/mL”, a análise forense. O químico pipetou 100 μL da solução contida no frasco e a diluiu em H2SO4 0,5 mol/L até atingir o volume de 10,0 mL. Após agitar a solução, essa foi colocada em uma cubeta de 1 cm e um espectro de UV-VIS foi registrado. O químico observou que o espectro obtido era qualitativamente similar ao espectro de referência da meperidina e que a absorvância a 257 nm era igual a 0,075.
Nessa situação, sabendo-se que a absortividade molar da meperidina a 257 nm é igual a 0,85 L × g-1 × cm-1 em solução ácida e que a sua massa molar é igual a 247,3 g/mol, julgue o item subseqüente.
O espectro de UV-VIS indica que o frasco cujo conteúdo foi analisado
contém, muito provavelmente, meperidina.
Considere a seguinte situação hipotética.
Uma enfermeira é suspeita de ter trocado deliberadamente o conteúdo de um frasco de remédio, retirando a droga nele contida e substituindo-a por solução salina. Um agente policial submeteu o frasco em questão, que continha no rótulo a informação “meperidina 20 mg/mL”, a análise forense. O químico pipetou 100 μL da solução contida no frasco e a diluiu em H2SO4 0,5 mol/L até atingir o volume de 10,0 mL. Após agitar a solução, essa foi colocada em uma cubeta de 1 cm e um espectro de UV-VIS foi registrado. O químico observou que o espectro obtido era qualitativamente similar ao espectro de referência da meperidina e que a absorvância a 257 nm era igual a 0,075.
Nessa situação, sabendo-se que a absortividade molar da meperidina a 257 nm é igual a 0,85 L × g-1 × cm-1 em solução ácida e que a sua massa molar é igual a 247,3 g/mol, julgue o item subseqüente.
A absorvância medida pelo químico indica que a concentração de
meperidina na solução analisada é realmente de 20 mg/mL, resultado
que isentaria a enfermeira de culpa.
Considere a seguinte situação hipotética.
Uma enfermeira é suspeita de ter trocado deliberadamente o conteúdo de um frasco de remédio, retirando a droga nele contida e substituindo-a por solução salina. Um agente policial submeteu o frasco em questão, que continha no rótulo a informação “meperidina 20 mg/mL”, a análise forense. O químico pipetou 100 μL da solução contida no frasco e a diluiu em H2SO4 0,5 mol/L até atingir o volume de 10,0 mL. Após agitar a solução, essa foi colocada em uma cubeta de 1 cm e um espectro de UV-VIS foi registrado. O químico observou que o espectro obtido era qualitativamente similar ao espectro de referência da meperidina e que a absorvância a 257 nm era igual a 0,075.
Nessa situação, sabendo-se que a absortividade molar da meperidina a 257 nm é igual a 0,85 L × g-1 × cm-1 em solução ácida e que a sua massa molar é igual a 247,3 g/mol, julgue o item subseqüente.
Admitindo que o químico tenha utilizado uma solução comercial de
ácido sulfúrico 49% em massa, de densidade igual a 1,39 g/mL, para
preparar a solução de H2SO4 usada nessa determinação, e sabendo que
M(H) = 1 g/mol, M(O) = 16 g/mol e M(S) = 32 g/mol, é correto
concluir que foi pipetado pelo químico menos de 5 mL dessa solução
para preparar 100 mL de solução de H2SO4 0,5 mol/L.
Sprays de ninidrina têm sido utilizados por peritos criminais para auxiliar na visualização de impressões digitais. A ninidrina reage com os aminoácidos da impressão digital e forma um produto azul-violeta, denominado púrpura de Ruhemann, que revela a impressão digital quando iluminado. A partir dessas informações, da reação mostrada acima e sabendo-se que M(H) = 1 g/mol, M(C) = 12 g/mol, M(O) = 16 g/mol, julgue o item a seguir, considerando que o volume molar de um gás ideal nas CNTP é igual a 22,7 L/mol.
O aminoácido mostrado na reação é um $-aminoácido secundário.
Sprays de ninidrina têm sido utilizados por peritos criminais para auxiliar na visualização de impressões digitais. A ninidrina reage com os aminoácidos da impressão digital e forma um produto azul-violeta, denominado púrpura de Ruhemann, que revela a impressão digital quando iluminado. A partir dessas informações, da reação mostrada acima e sabendo-se que M(H) = 1 g/mol, M(C) = 12 g/mol, M(O) = 16 g/mol, julgue o item a seguir, considerando que o volume molar de um gás ideal nas CNTP é igual a 22,7 L/mol.
Pelo menos uma das substâncias mostradas na reação é uma amida.
Sprays de ninidrina têm sido utilizados por peritos criminais para auxiliar na visualização de impressões digitais. A ninidrina reage com os aminoácidos da impressão digital e forma um produto azul-violeta, denominado púrpura de Ruhemann, que revela a impressão digital quando iluminado. A partir dessas informações, da reação mostrada acima e sabendo-se que M(H) = 1 g/mol, M(C) = 12 g/mol, M(O) = 16 g/mol, julgue o item a seguir, considerando que o volume molar de um gás ideal nas CNTP é igual a 22,7 L/mol.
A reação entre o produto de desidratação da ninidrina e o
aminoácido pode ser corretamente classificada como uma adição
nucleofílica ao grupo carbonila.
Sprays de ninidrina têm sido utilizados por peritos criminais para auxiliar na visualização de impressões digitais. A ninidrina reage com os aminoácidos da impressão digital e forma um produto azul-violeta, denominado púrpura de Ruhemann, que revela a impressão digital quando iluminado. A partir dessas informações, da reação mostrada acima e sabendo-se que M(H) = 1 g/mol, M(C) = 12 g/mol, M(O) = 16 g/mol, julgue o item a seguir, considerando que o volume molar de um gás ideal nas CNTP é igual a 22,7 L/mol.
A conversão de 1 g de ninidrina em púrpura de Ruhemann a 0ºC
e 1 atm lança na atmosfera menos de 200 mL de CO2,
admitindo-se um comportamento ideal do gás e um sistema aberto.
A respeito dos conceitos relativos à química inorgânica, julgue o seguinte item.
O gráfico abaixo permite concluir que a eletronegatividade é uma propriedade periódica.
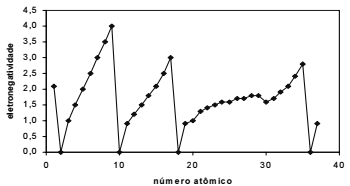
A respeito dos conceitos relativos à química inorgânica, julgue o seguinte item.
Se uma quantidade significativa de cal virgem (CaO) for
adicionada a uma solução aquosa de fenolftaleína, o resultado será
uma solução incolor.
A respeito dos conceitos relativos à química inorgânica, julgue o seguinte item.
Compostos iônicos são normalmente sólidos à temperatura
ambiente, possuem pontos de fusão geralmente altos e são bons
condutores de corrente elétrica quando fundidos ou em solução
aquosa. A maioria dos compostos iônicos é solúvel em água e
insolúvel em solventes apolares orgânicos.
A respeito dos conceitos relativos à química inorgânica, julgue o seguinte item.
O complexo neutro Co(NH3)3(NO2)3 possui apenas dois isômeros.
No que concerne à titulometria, julgue o item que se segue.
O permanganato de potássio tem sido a cada dia mais utilizado
como titulante em volumetria de oxirredução, pelo seu alto poder
oxidante, além de apresentar grande precisão nas titulações.
No que concerne à titulometria, julgue o item que se segue.
O excepcional poder quelante do EDTA oferece uma vantagem e
uma desvantagem no que se refere a titulações complexométricas.
Se, por um lado, ele torna o EDTA um reagente extremamente
versátil, que pode ser utilizado na determinação de diversos
cátions di, tri e tetravalentes, por outro lado, faz dele um titulante
muito pouco seletivo. Essa desvantagem pode ser minimizada
mediante um controle preciso do pH.

