Questões de Concurso Público FUB 2011 para Químico - Específicos
Foram encontradas 50 questões
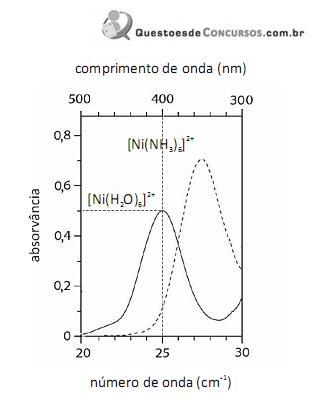


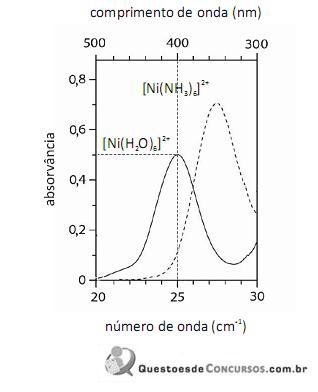

Considerando-se a teoria do campo cristalino e os espectros acima apresentados, é correto afirmar que a água consiste em um ligante de campo mais fraco que a amônia.
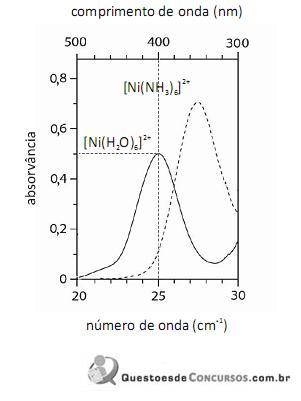

Em face dos espectros acima apresentados, é correto concluir que o módulo do valor da energia de estabilização do campo cristalino (EECC) para o complexo
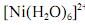 é superior a 4,0×10-19 J.
é superior a 4,0×10-19 J. 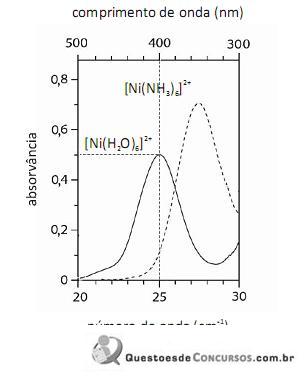

A análise espectroscópica do
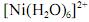 mostra que a razão entre o número de fótons com comprimento de onda igual a 400 nm que atinge o transdutor e o número desses fótons que atinge a amostra é maior do que 0,40.
mostra que a razão entre o número de fótons com comprimento de onda igual a 400 nm que atinge o transdutor e o número desses fótons que atinge a amostra é maior do que 0,40. 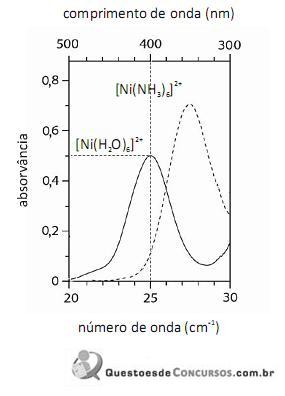

O fato de os espectros acima apresentarem largas bandas de absorção, em vez de linhas ou picos estreitos, demonstra que o equipamento utilizado não possuía monocromador.
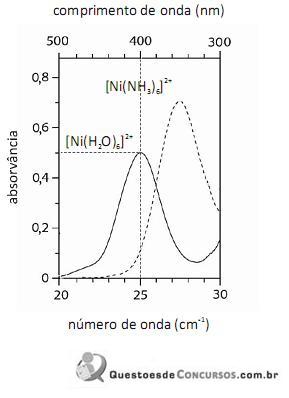

De acordo com a lei de Beer, infere-se do espectro do complexo
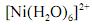 que, para uma radiação com comprimento de onda igual a 400 nm, a absortividade molar é maior que
que, para uma radiação com comprimento de onda igual a 400 nm, a absortividade molar é maior que 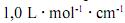 .
. 
Com base nessas informações, julgue os itens que se seguem.
Caso, na reação acima, a coloração amarela torne-se mais intensa ao se aumentar a temperatura do sistema, é correto concluir que a reação será endotérmica no sentido da formação de
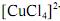 .
. 
Com base nessas informações, julgue os itens que se seguem.
Considerando-se que, a uma dada temperatura T, o sistema acima descrito, no equilíbrio, apresente uma quantidade de íons
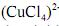 igual à quantidade de íons
igual à quantidade de íons 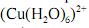 e o coeficiente de atividade de todas as espécies iguais a 1, é correto concluir que a concentração de íons
e o coeficiente de atividade de todas as espécies iguais a 1, é correto concluir que a concentração de íons 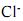 será superior a 0,50.
será superior a 0,50. 
Com base nessas informações, julgue os itens que se seguem.
Os complexos de metais de transição com configuração eletrônica d9 , tais como o complexo
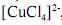 , caracterizam-se pela geometria quadrado planar.
, caracterizam-se pela geometria quadrado planar. Considerando as informações acima e que os desvios padrão sejam
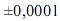 g, para uma simples leitura na balança utilizada,
g, para uma simples leitura na balança utilizada,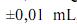 e , para uma leitura de menisco no balão, julgue os próximos itens.
e , para uma leitura de menisco no balão, julgue os próximos itens.Caso a solução de biftalato preparada seja usada, posteriormente, na padronização de uma solução básica, a presença de impurezas no biftalato usado para a preparação de sua solução gerará um erro aleatório que, consequentemente, afetará a precisão dos resultados obtidos durante a padronização.
Preparou-se 100 mL de uma solução padrão de biftalato de potássio, de acordo com o seguinte procedimento: (i) pesagem de um béquer vazio em uma balança analítica; (ii) pesagem do béquer contendo 2,0000 g do biftalato na mesma balança; (iii) dissolução do biftalato, por meio da adição de água suficiente ao béquer; (iv) transferência de todo o conteúdo do béquer para um balão volumétrico de 100,00 mL; (v) preenchimento do balão com água até o menisco.
Considerando as informações acima e que os desvios padrão sejam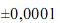 g, para uma simples leitura na balança utilizada, e
g, para uma simples leitura na balança utilizada, e 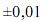 mL, para uma leitura de menisco no balão, julgue o próximo item.
mL, para uma leitura de menisco no balão, julgue o próximo item.
O desvio padrão relativo para a concentração da solução de biftalato de potássio preparada é maior que 1,0×10-4 .
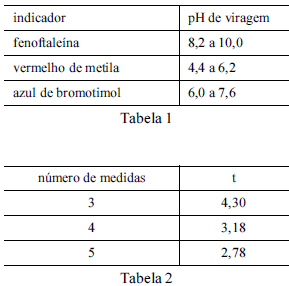
Considere que uma solução de NaOH foi padronizada por meio da titulação, em quadruplicata, com 20,00 mL de uma solução padrão de biftalato de potássio 0,1000 mol/L e que a concentração média encontrada para a solução de NaOH foi de 0,080 mol/L, com uma estimativa do desvio padrão de ±0,002 mol/L. Considere, ainda, a tabela 1, em que é apresentado o pH de viragem de alguns indicadores ácido-base, e a tabela 2, em que são apresentados os valores do parâmetro t de student para uma probabilidade de 95%. Com base nessas informações, julgue os itens seguintes.
A partir dos resultados obtidos, pode-se inferir que o volume
médio da solução de NaOH gasto na titulação é maior que
22,0 mL.
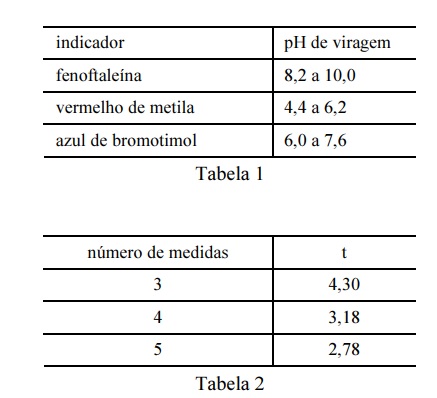
Considere que uma solução de NaOH foi padronizada por meio da titulação, em quadruplicata, com 20,00 mL de uma solução padrão de biftalato de potássio 0,1000 mol/L e que a concentração média encontrada para a solução de NaOH foi de 0,080 mol/L, com uma estimativa do desvio padrão de ±0,002 mol/L. Considere, ainda, a tabela 1, em que é apresentado o pH de viragem de alguns indicadores ácido-base, e a tabela 2, em que são apresentados os valores do parâmetro t de student para uma probabilidade de 95%.
Com base nessas informações, julgue os itens seguintes.
Considerando-se a inexistência de erros sistemáticos, é correto afirmar que a probabilidade de que o valor real da concentração de NaOH esteja no intervalo compreendido entre 0,078 e 0,082 será maior que 95%.

Considere que uma solução de NaOH foi padronizada por meio da titulação, em quadruplicata, com 20,00 mL de uma solução padrão de biftalato de potássio 0,1000 mol/L e que a concentração média encontrada para a solução de NaOH foi de 0,080 mol/L, com uma estimativa do desvio padrão de ±0,002 mol/L. Considere, ainda, a tabela 1, em que é apresentado o pH de viragem de alguns indicadores ácido-base, e a tabela 2, em que são apresentados os valores do parâmetro t de student para uma probabilidade de 95%.
Com base nessas informações, julgue os itens seguintes
Entre os indicadores apresentados na tabela 1, o mais
adequado à titulação em questão é o vermelho de metila.
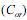 e na fase aquosa
e na fase aquosa 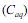 , quando atingido o
, quando atingido o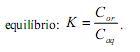
Dois estudantes realizaram a extração de um composto, a partir de uma solução aquosa com a concentração do composto igual a 0,0100 mol/L. O estudante A realizou uma única extração, utilizando 100 mL da solução aquosa e 100 mL de 1-octanol, e o estudante B utilizou o mesmo volume da solução aquosa, mas realizou duas extrações consecutivas, cada uma com 50 mL de 1-octanol.
Considerando o conjunto de informações apresentado acima e que o coeficiente de partição do composto no sistema 1-octanol/água seja igual a 2,0, julgue os itens que se seguem.
Caso o composto seja um ácido que sofra ionização em água, então, a fração extraída será tanto maior quanto mais elevado for o pH da fase aquosa.
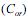 e na fase aquosa
e na fase aquosa 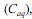 , quando atingido o
, quando atingido o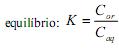
Dois estudantes realizaram a extração de um composto, a partir de uma solução aquosa com a concentração do composto igual a 0,0100 mol/L. O estudante A realizou uma única extração, utilizando 100 mL da solução aquosa e 100 mL de 1-octanol, e o estudante B utilizou o mesmo volume da solução aquosa, mas realizou duas extrações consecutivas, cada uma com 50 mL de 1-octanol.
Considerando o conjunto de informações apresentado acima e que o coeficiente de partição do composto no sistema 1-octanol/água seja igual a 2,0, julgue os itens que se seguem.
Considerando-se que o composto não sofra qualquer reação adicional nas fases aquosa e orgânica, é correto inferir que a porcentagem desse composto extraída pelo estudante A será maior que 80%.
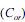 e na fase aquosa
e na fase aquosa 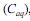 , quando atingido o
, quando atingido o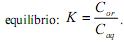
Dois estudantes realizaram a extração de um composto, a partir de uma solução aquosa com a concentração do composto igual a 0,0100 mol/L. O estudante A realizou uma única extração, utilizando 100 mL da solução aquosa e 100 mL de 1-octanol, e o estudante B utilizou o mesmo volume da solução aquosa, mas realizou duas extrações consecutivas, cada uma com 50 mL de 1-octanol.
Considerando o conjunto de informações apresentado acima e que o coeficiente de partição do composto no sistema 1-octanol/água seja igual a 2,0, julgue os itens que se seguem.
A fração do composto extraída pelo estudante B será maior que a extraída pelo estudante A.
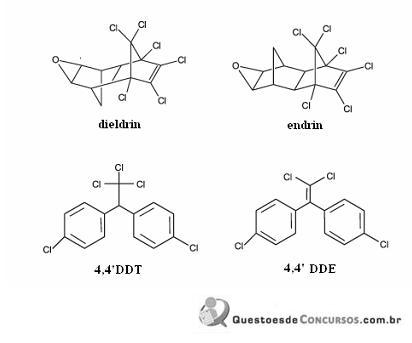
Considerando a figura acima, que ilustra as estruturas químicas de quatro pesticidas, julgue os itens que se seguem.
O composto 4,4’DDE consiste no principal produto da reação do 4,4’DDT com KOH, que se processa via mecanismo de eliminação bimolecular.
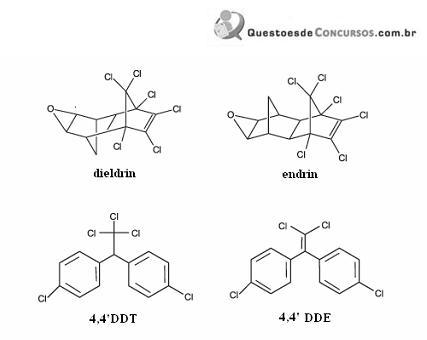
Considerando a figura acima, que ilustra as estruturas químicas de quatro pesticidas, julgue os itens que se seguem.
A molécula de dieldrin apresenta a função éter.
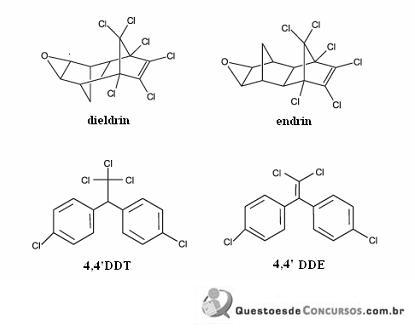
Considerando a figura acima, que ilustra as estruturas químicas de quatro pesticidas, julgue os itens que se seguem.
O composto 4,4’DDE denomina-se 1,1-di(p-clorobenzil)-eteno.