Questões de Concurso Público IFF 2018 para Professor - Química I
Foram encontradas 30 questões
Texto 19A1AAA
O titânio, um metal de transição do “bloco d” da tabela periódica, é bastante empregado em ligas metálicas devido a sua elevada resistência mecânica e baixa tendência à corrosão, além da baixa densidade. Ele é obtido a partir, principalmente, da ilmenita (FeTiO3) e do rutilo (TiO2).
Texto 19A1AAA
O titânio, um metal de transição do “bloco d” da tabela periódica, é bastante empregado em ligas metálicas devido a sua elevada resistência mecânica e baixa tendência à corrosão, além da baixa densidade. Ele é obtido a partir, principalmente, da ilmenita (FeTiO3) e do rutilo (TiO2).
Texto 19A1AAA
O titânio, um metal de transição do “bloco d” da tabela periódica, é bastante empregado em ligas metálicas devido a sua elevada resistência mecânica e baixa tendência à corrosão, além da baixa densidade. Ele é obtido a partir, principalmente, da ilmenita (FeTiO3) e do rutilo (TiO2).
Texto 19A1AAA
O titânio, um metal de transição do “bloco d” da tabela periódica, é bastante empregado em ligas metálicas devido a sua elevada resistência mecânica e baixa tendência à corrosão, além da baixa densidade. Ele é obtido a partir, principalmente, da ilmenita (FeTiO3) e do rutilo (TiO2).
Os elementos de transição do “bloco d” da tabela periódica têm como característica formar complexos com colorações e propriedades magnéticas variadas. Por exemplo, o cobalto pode formar os íons complexos [CoCℓ6]3 e [Co(NH3)6]3+. O [CoCℓ6]3 é um complexo de spin alto com coloração laranja; por sua vez, o [Co(NH3)6]3+ é um complexo de spin baixo e coloração amarela.
Tendo como referência as informações precedentes e considerando que os compostos diamagnéticos apresentam todos seus elétrons emparelhados e os compostos paramagnéticos possuem elétrons desemparelhados, assinale a opção correta, de acordo com a teoria do campo cristalino.
Texto 19A1BBB
Um caminhão contendo ácido sulfúrico (H2SO4) concentrado tombou e seu conteúdo vazou sobre a rodovia e atingiu um pequeno lago nas imediações. Nos dias que se seguiram ao acidente, a análise da água do lago detectou uma concentração analítica do ácido igual a 1,00 • 10 2 mol/L. Visando-se a neutralizar a acidez causada na água do lago, um produto químico foi utilizado.
Para responder à questão, considere que a solução formada tenha comportamento ideal, que inicialmente a água se encontrava com pH neutro, que a primeira ionização do ácido sulfúrico seja completa e a segunda ionização seja parcial, e assuma 0,30 como o valor de log 2.
Texto 19A1BBB
Um caminhão contendo ácido sulfúrico (H2SO4) concentrado tombou e seu conteúdo vazou sobre a rodovia e atingiu um pequeno lago nas imediações. Nos dias que se seguiram ao acidente, a análise da água do lago detectou uma concentração analítica do ácido igual a 1,00 • 10 2 mol/L. Visando-se a neutralizar a acidez causada na água do lago, um produto químico foi utilizado.
Para responder à questão, considere que a solução formada tenha comportamento ideal, que inicialmente a água se encontrava com pH neutro, que a primeira ionização do ácido sulfúrico seja completa e a segunda ionização seja parcial, e assuma 0,30 como o valor de log 2.
Texto 19A1BBB
Um caminhão contendo ácido sulfúrico (H2SO4) concentrado tombou e seu conteúdo vazou sobre a rodovia e atingiu um pequeno lago nas imediações. Nos dias que se seguiram ao acidente, a análise da água do lago detectou uma concentração analítica do ácido igual a 1,00 • 10 2 mol/L. Visando-se a neutralizar a acidez causada na água do lago, um produto químico foi utilizado.
Para responder à questão, considere que a solução formada tenha comportamento ideal, que inicialmente a água se encontrava com pH neutro, que a primeira ionização do ácido sulfúrico seja completa e a segunda ionização seja parcial, e assuma 0,30 como o valor de log 2.
O biogás é constituído principalmente por CH4 (55% a 80% V/V) e CO2. Antes de ser empregado como combustível, ou biogás bruto deve passar por um pré-tratamento para ativar-se ao aumento do teor de CH4. Esse pré-tratamento pode envolver diversos métodos, que exploram como diferentes componentes físicos-químicos dos componentes para separá-los. Como exemplos, pode-se citar:
• absorção física, em que são exploradas como diferentes solubilidades dos componentes em um dado solvente;
• uma condensação fracionada, em que são exploradas como diferentes temperaturas de condensação dos componentes;
• uma seleção por membranas semipermeáveis, que são exploradas como diferentes dimensões das moléculas dos componentes para promover uma espécie de filtragem.
A respeito das relações entre as estruturas moleculares e as
propriedades que permitem a separação do CH4 e do CO2 durante
o pré-tratamento do biogás, assinale a opção correta.
Texto 19A1CCC
Além do emprego como combustível, o CH4 pode ser utilizado como insumo para a síntese de diversos compostos químicos. A seguir, destaca-se a sua oxidação parcial para a síntese de metanol, reação esta que pode ser catalisada por um óxido metálico.
CH4 + ½ O2 ⇌ CH3OH
Texto 19A1CCC
Além do emprego como combustível, o CH4 pode ser utilizado como insumo para a síntese de diversos compostos químicos. A seguir, destaca-se a sua oxidação parcial para a síntese de metanol, reação esta que pode ser catalisada por um óxido metálico.
CH4 + ½ O2 ⇌ CH3OH
O dióxido de carbono gerado em estações espaciais pode ser convertido em oxigênio pela reação com o superóxido de potássio, conforme a equação a seguir.
2CO2(g) + 4KO2(s) → 2K2CO3(s) + 3O2(g)
Tendo como referência a reação precedente, assinale a opção que apresenta a massa exata de KO2 necessária para a conversão total de 11,2 L de CO2 em oxigênio nas condições normais de temperatura e pressão (CNTP), considerando que o valor do volume molar de um gás ideal nas CNTP seja 22,4 L e que todos os gases comportem-se idealmente.
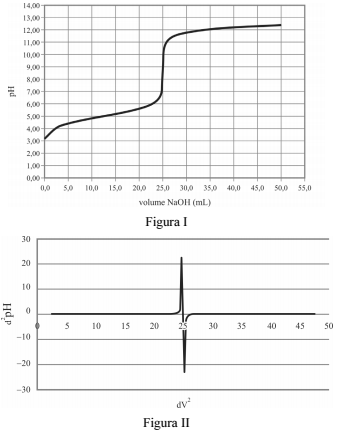
A figura I precedente mostra a variação do pH em função do volume de NaOH na titulação de 50,0 mL de uma solução de um ácido com uma solução de NaOH a 0,05 mol/L. A figura II mostra a segunda derivada da curva da figura I.
Considerando essas informações, assinale a opção correta a respeito
de volumetria e dos assuntos que esse tema suscita.
As soluções de íons cério (IV) e de íons permanganato são reagentes oxidantes fortes muito utilizados na titulação de amostras que contenham ferro. A tabela a seguir mostra as semirreações e os correspondentes potenciais padrão de eletrodo.

A partir das informações precedentes, assinale a opção correta a
respeito de eletroquímica e dos assuntos suscitados por esse tema.
A tabela a seguir lista as reações de combustão do carbono sólido C(s) como grafite, do gás hidrogênio H2(g) e do gás metano CH4(g). As variações de entalpia (ΔH) para essas reações também estão listadas na tabela.
reação ΔH
C(s) + O2(g) → CO2(g) x
H2(g) + ½O2(g) → H2O(l) y
CH4(g) + 2O2(g) → CO2(g) + 2H2O(l) z
sal ΔHsol (kJ/mol) solubilidade em água a 18 ºC (g/100 mL)
LiF +32 0,3
KF +2 92,3
RbF 3 130,6
Considerando os dados na tabela precedente, que lista alguns sais
e seus respectivos valores de entalpia de dissolução (ΔHsol) e
solubilidade, assinale a opção correta a respeito de soluções e
propriedades de soluções.
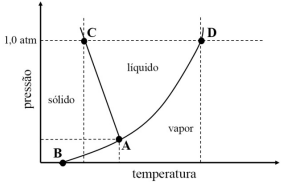
Considerando o gráfico precedente, que ilustra o diagrama de fases
para um composto molecular puro, assinale a opção correta.