Questões de Concurso Público UFPI 2023 para Técnico de Laboratório - Química
Foram encontradas 2 questões
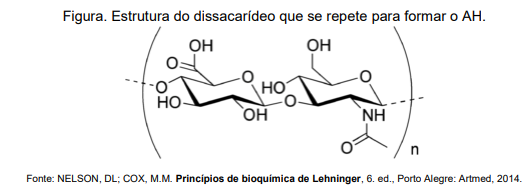
O AH é altamente hidrofílico e capaz de reter grandes quantidades de água, o que lhe confere propriedades viscoelásticas e lubrificantes. Na pele, por exemplo, ele é responsável por manter a hidratação e elasticidade, além de ajudar a preencher o meio extracelular, o que contribui para a uniformidade da superfície cutânea.
Sobre a química do AH e a partir dos seus conhecimentos, assinale a opção CORRETA:
Na sequência o iodo foi titulado com tiossulfato de sódio a 0,100 mol/L até o ponto final, com o gasto de 30,00 mL de titulante. Esta última reação foi: I2 + 2 S2O2-3(aq) ➝ 2 I-(aq) + S4O2-6(aq).
Diante das informações, assinale a opção que mostra A PORCENTAGEM EM MASSA DE ZINCO NA AMOSTRA de latão: Dados: massas molares (g/mol): Cu = 63,5; Zn = 65,4.