Questões de Concurso Público SEDUC-GO 2010 para Professor - Química
Foram encontradas 19 questões
O processo eletroquímico de corrosão de materiais metálicos, como o ferro, pode ser representado pelas seguintes equações químicas:
4H2O(l) + 2Fe+3 (aq) ⇋ 6H+ (aq) + Fe2O3.H2O(s)
2Fe+2(aq) + 1/2O2(g) + 2H+ (aq) ⇋ 2Fe+3(aq) + H2O(l)
2Fe(s) + O2(g) + 4H+ (aq) ⇋ 2Fe+2(aq) + 2H2O(l)
Assim, quando essas equações são somadas, resultarão
na equação total balanceada da ferrugem. Os coeficientes
da equação balanceada para o Fe(s), gás oxigênio, água e
óxido de ferro (III) hidratado são, respectivamente:
Durante uma aula de experimentação no laboratório da escola, um professor solicitou aos alunos que preparassem soluções utilizando um alvejante comercial e vinagre. De cada solução preparada, foram separadas duas amostras em diferentes tubos de ensaio e adicionadas gotas de indicadores, conforme a tabela a seguir.
Tubo de Ensaio
I - Alvejante
II - Vinagre
III - Alvejante
IV - Vinagre
Indicador adicionado
Extrato de repolho roxo
Extrato de repolho roxo
Verde de bromocresol
Verde de bromocresol
As cores observadas após a adição dos indicadores no tubos
de ensaio I, II, III e IV são, respectivamente,
Observe a tabela a seguir.
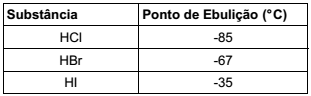
Forças intermoleculares mais fortes levam a pontos de ebulição mais altos, quando se aumentam os momentos dipolo e a
energia de interação dipolo-dipolo. No entanto, tal fator não é
observado nas substâncias apresentadas na tabela. A explicação para isso reside no fato de que
Observe a reação a seguir.
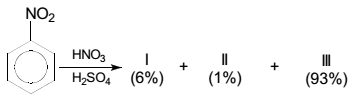
De acordo com as características orientadoras do grupo
nitro em reações de substituição no anel benzênico, o produto
formado em maior porcentagem será
Nos diversos refrigerantes, o ácido fosfórico é utilizado como acidulante. Em cada lata de refrigerante são utilizados aproximadamente 35 mg de ácido fosfórico. Aproximadamente, quantas latas de refrigerante serão necessárias para que esse ácido, adicionado ao bicarbonato ácido de sódio, produza CO2 suficiente para encher um balão de festa com um volume de 3 litros?
(Dados: Pressão = 1 atm; Temperatura
= 25° C; R = 0,082 atm L mol -1
K
-1)