Questões de Concurso Público UFG 2017 para Técnico de Laboratório/Área Química
Foram encontradas 29 questões
No processo de mineração do minério de ferro, aminas de éter são empregadas para separar a sílica do minério de ferro.
Dentre as alternativas a seguir, a que contém a fórmula molecular de um éter de amina primária é:
O esquema a seguir mostra a separação cromatográfica das substâncias I, II e III, utilizando sílica (SiO2) como fase estacionária. Cada faixa representa uma substância.
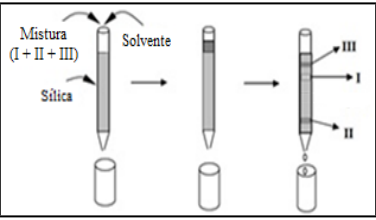
A mistura analisada é composta de substâncias, com pesos moleculares equivalentes, das classes: álcool, amina e hidrocarboneto. Com base nestas informações, as substâncias I, II e III representam, respectivamente, compostos das classes:
Considere que um frasco de quartzo de alta pressão com volume de 80 mL está inserido em um forno de micro-ondas e suponha que, dentro dele, exista apenas uma fase de vapor de água a 280 oC e 80 bar. Se essa amostra de água for resfriada até 4 oC e 1 atm, qual será o volume, em mL, de líquido?

Os equipamentos e vidrarias que seguem são comumente encontrados em um laboratório de Química. Considere-os para responder à questão.
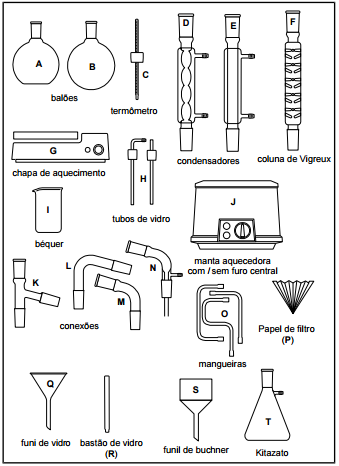
Os equipamentos e vidrarias que seguem são comumente encontrados em um laboratório de Química. Considere-os para responder à questão.

O texto a seguir foi adaptado de Quim. Nova, v. 39, 732- 740, 2016.
“Nos ambientes aquáticos, a concentração de fosfatos na coluna de água é dependente de alguns fatores, como o par redox Fe(II)/Fe(III), uma vez que nas camadas superficiais sua associação com os oxi-hidróxidos de Fe(III) formam compostos que apresentam baixa solubilidade e migram para camadas mais profundas (sedimento). Nessas camadas os oxi-hidróxidos de Fe(II), mais solúveis que os compostos de Fe(III, são formados, com a liberação do fosfato, estabelecendo um ciclo onde o fósforo migra novamente para as camadas superficiais.”
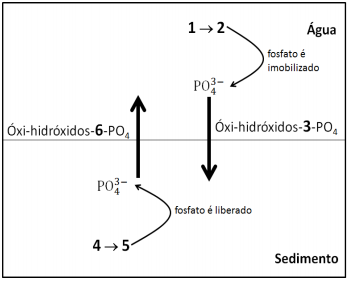
O equilíbrio químico descrito no texto evidencia que os
números 1, 2, 3, 4, 5 e 6 são:
A figura a seguir, adaptada da revista Quim. Nova, v. 38, 1265-1272, 2015, representa o processo de degradação fotocalítica do azul de metileno obtida com uma amostra de CaFe em diferentes condições.
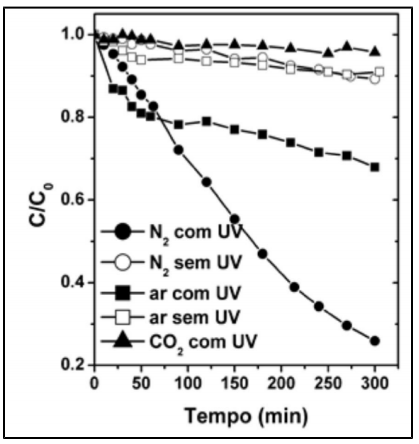
Com base nessa figura, a condição na qual a velocidade inicial
é maior é:
Em um experimento, para determinar a massa atômica de um elemento, foi constatado que a massa determinada era 140 vezes mais pesada do que um átomo de hidrogênio. Sabendo que o número de prótons é igual a 59, determine o número de átomos em um 1 kg de amostra desse elemento:

A equação  descreve a reação entre dois
gases cuja avaliação é mencionada na tabela que se segue.
descreve a reação entre dois
gases cuja avaliação é mencionada na tabela que se segue.
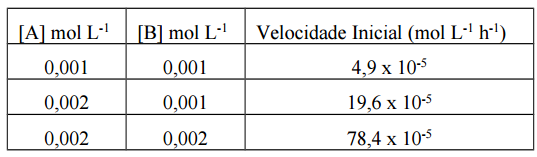
De acordo com os dados apresentados, a constante de
velocidade nessa reação, em mol-3 L3
h-1, é:

Em uma aula experimental de química, três soluções foram submetidas à destilação. O gráfico a seguir representa o comportamento dessas soluções.
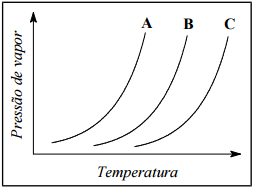
Este gráfico evidencia o ponto de ebulição