Questões de Concurso Público SABESP 2018 para Químico 01
Foram encontradas 50 questões
Atenção: Para responder à questão, considere a curva de titulação abaixo.

Oxirredução é um processo em que ocorre transferência de elétrons entre as espécies no decorrer de uma reação química.
K2Cr2O7 (aq) + 4 H2SO4 (aq) + 3 C2H5OH (aq) → 3 C2H4O (g) + K2SO4 (aq) + Cr2 (SO4)3 (aq) + 7 H2O (l)
Considerando a reação entre dicromato de potássio (K2Cr2O7) com álcool etílico (C2H5OH) na presença de ácido sulfúrico
(H2SO4),
O rompimento de uma adutora de 700 mm de diâmetro na tarde de quinta-feira do dia 22 de março de 2018, localizada no quilômetro 59 da via marginal da Anhanguera, afetou o abastecimento de água em alguns bairros de Jundiaí (SP).
(Adaptado de: https://g1.globo.com)
Esse evento pode ocorrer devido à corrosão eletroquímica. Em tubulações de ferro é adequado fazer proteção catódica, utilizando ânodos fixados na tubulação que fica submersa no solo.
Considere os seguintes potenciais de redução, a 25,0 °C:
Fe2+(aq) + 2 e− ⇋ Fe(s) Eo = −0,440 V
Cu2+ (aq) + 2 e− ⇋ Cu(s) Eo = +0,337 V
Sn2+ (aq) + 2 e− ⇋ Sn(s) Eo = −0,136 V
Ni2+ (aq) + 2 e− ⇋ Ni(s) Eo = −0,250 V
Co2+ (aq) + 2 e− ⇋ Co(s) Eo = −0,277 V
Zn2+ (aq) + 2 e− ⇋ Zn(s) Eo = −0,763 V
O metal mais apropriado como ânodo é o
Considere uma solução aquosa 0,1 mol L−1 contendo os cátions Sr2+, Ca2+, Ba2+, Ra2+ e Pb2+.
Dadas as constantes do produto de solubilidade (KPS):
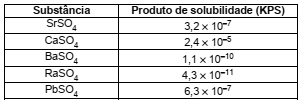
Se íons sulfato (SO2-4) forem gradualmente adicionados à solução acima,
Tratamentos a baixo custo para descarte adequado de efluentes industriais são alvos de buscas incessantes por engenheiros e outros profissionais. O uso de alguns resíduos vegetais em processos de coagulação e na remoção de íons cádmio de soluções aquosas por processos de adsorção, que seriam a princípio descartados em aterros sanitários, vem sendo utilizado em saneamento básico, podendo constituir uma alternativa viável de baixo custo e ambientalmente segura para a remoção de cátions metálicos tóxicos presentes em corpos d’água.
Este texto refere-se a
Nas estações de tratamento de água, uma das principais etapas para obtenção de água potável consiste na eliminação das impurezas que se encontram em suspensão, que pode ser realizada a partir da adição de sulfato de alumínio, Aℓ2(SO4)3, e de hidróxido de cálcio, Ca(OH)2, à superfície da água a ser tratada. O hidróxido de alumínio produzido atua como floculante, arrastando impurezas sólidas para o fundo do tanque no processo de decantação e, em seguida, o sobrenadante é filtrado e desinfetado. O esquema simplificado mostra as etapas do tratamento de água utilizado pelas estações convencionais, para transformar água captada dos reservatórios naturais em água potável.
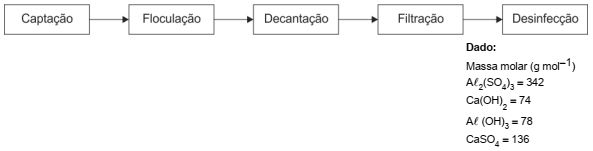
Em um teste piloto de tratamento de 0,50 m3 de água, foram adicionados 3,42 kg de sulfato de alumínio e 0,50 kg de hidróxido
de cálcio. Admitindo que não haja variação de volume é correto afirmar que