Questões de Concurso Público UNILAB 2019 para Técnico de Laboratório - Química
Foram encontradas 50 questões
MnO4- (aq) + Fe2+(aq) + H+(aq) → Fe3+(aq) + Mn2+(aq) + H2O(l)
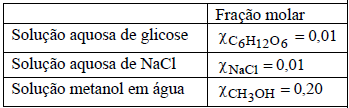
O quadro abaixo contem informações de três amostras a 25°C:
Considere as seguintes semi-reações e assinale a alternativa com a afirmação correta.

Analise as informações a seguir com relação a boas práticas de laboratório:
I. Em teste de aquecimento com tubo de ensaio, o mesmo deve estar preenchido até no máximo um terço de seu volume.
II. Em uma titulação, estudantes canhotos devem operar a bureta com a mão esquerda e manusear o erlenmeyer com a mão direita.
III. Em uma pipetagem, deve-se soprar o restante do líquido que fica na ponta da pipeta para o recipiente.
IV. A bureta deve ser sempre preenchida até a marca do zero antes de cada experimento de titulação.
Com relação as afirmações acima, assinale o item que representa o(s) procedimento(s) recomendado(s).
I. Algumas gotas da solução do tubo 1 foram adicionadas a um certo volume de solução do tubo 2. Não foi observado reação aparente, no entanto houve aquecimento do tubo.
II. Algumas gotas da solução do tubo 1 foram adicionadas a um certo volume de solução do tubo 3. Foi observada a formação de gás.
Com base nas informações, pode-se concluir que as soluções presentes nos tubos 1, 2 e 3 são, respectivamente:
I. 0,010 mol de CaCl2 II. 0,010 mol de KNO3 III. 0,010 mol de CO(NH3)2 IV. 0,020 mol de CaCl2 V. 0,020 mol de KNO3
A solução que produzirá o maior abaixamento na temperatura de fusão da água será a:
A figura abaixo representa o resultado de uma cromatografia em papel para uma série de substâncias, usando como fase móvel uma mistura de ácido butanoico/ácido acético.
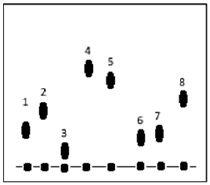
Com base na análise do cromatograma, pode-se afirmar que: