Questões de Concurso Público UFVJM-MG 2017 para Técnico em Química
Foram encontradas 5 questões
A concentração do hidróxido de sódio (NaOH) pode ser determinada via titulação por uma solução-padrão de ácido clorídrico (HCl). Considere que nesse processo de titulação foram consumidos 25 mL de HCl 0,1 mol/L.
Sabendo que o volume da base é de 50 mL, é correto afirmar que a concentração NaOH em gramas por litro é igual a:
A lei de absorção, também conhecida como lei de Beer-Lambert ou somente lei de Beer, diz quantitativamente como a grandeza da atenuação depende da concentração das moléculas absorventes e da extensão do caminho sobre o qual ocorre a absorção.
Considere, hipoteticamente, que uma solução 0,10 mol/L de permanganato de potássio (KMnO4 ) apresenta uma absorbância igual a 0,340, quando medida em uma célula de 2,0 cm no comprimento de 525 nm.
Nessas condições, é correto afirmar que a absortividade molar do KMnO4 é igual a:
Considere que no preparo de uma solução de HCl 0,1 mol/L um técnico utiliza 4,5 mL da solução de estoque do reagente concentrado. A solução de estoque tem as seguintes especificações:

Nessas condições, e para garantir uma concentração
mais próxima possível daquela que o técnico pretende,
é correto afirmar que o balão volumétrico utilizado para
o preparo dessa solução é de:
A curva para a titulação de um ácido fraco por uma base forte é muito similar no formato àquela para a titulação de um ácido forte por uma base forte. Quando ácidos fracos contêm mais de um átomo de hidrogênio ionizável, como no ácido fosfórico (H3PO3 ), a reação com OH- ocorre em uma série de etapas.
Considere o gráfico a seguir, que representa a curva de titulação para a reação de 50 mL de 0,1 mol/L de H3PO3 com 0,1 mol/L de NaOH.
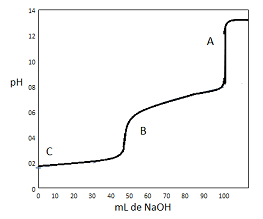
Segundo a curva de titulação, as espécies químicas A, B
e C são, respectivamente:
Muitos íons metálicos formam complexos estáveis, solúveis em água, com muitas aminas terciárias. A formação desses complexos serve como base nas titulações complexométricas de íons metálicos.
Sobre as titulações complexométricas, assinale a alternativa INCORRETA.