Questões de Concurso Público INB 2018 para Técnico em Química
Foram encontradas 19 questões
COLUNA I 1. Hidrogênio 2. Oxigênio 3. Nitrogênio 4. Flúor
COLUNA II ( ) É encontrado em duas formas moleculares gasosas, sendo que uma delas é extremamente tóxica e a outra é um não combustível pouco solúvel em água. ( ) É encontrado na forma de gás e extremamente importante na composição química das proteínas, que são moléculas presentes em todos os organismos vivos. ( ) Na forma molecular, é um gás, à temperatura ambiente, amarelo pálido e apresenta elevada reatividade. ( ) É encontrado na natureza como gás diatômico incolor e inflamável muito útil na produção de gás amoníaco.
Assinale a sequência CORRETA.
6NH4 ClO4 (s) + 10Al (s) → 5Al2 O3 (s) + 3N2 (g) + 6HCl (g) + 9H2O (g)
Considerando que se colocou para reagir 1 kg do perclorato de amônio com 1 kg do alumínio, quanto, aproximadamente, de massa, em gramas, do óxido foi produzido na reação?
I. Preparou a solução de NaOH. II. Pesou o padrão primário em um recipiente adequado para titulação. III. Titulou o padrão primário com o NaOH.
Sobre os procedimentos I, II e III, pode-se afirmar que as vidrarias mais adequadas para tais execuções foram, respectivamente:

O volume extraído da solução de estoque foi de 5 mililitros. Considerando que o técnico preparou uma solução de 0,12 mol/L, qual é o volume mais adequado do recipiente que foi utilizado para o preparo dessa solução?
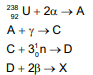
Nessas condições, é correto afirmar que o elemento X é a espécie:
I. Um exemplo de erro sistemático é quando se prepara uma solução com um balão volumétrico incorretamente calibrado,
PORQUE
II. esse tipo de erro surge por um problema consistente na técnica de um analista, em um instrumento ou em um procedimento.
A respeito dessas asserções, assinale a alternativa CORRETA.
X (s) / X2+ (1,05 mol/L) // Y2+ (1,10 mol/L) / Y (s)
Sobre a notação descrita, foram feitas as seguintes afirmações. I. As duas barras (//) indicam a ponte salina. II. X representa o eletrodo do anodo e Y, o eletrodo do catodo para reações espontâneas. III. O potencial da pilha se encontra em condição diferente do padrão.
Estão corretas as afirmações:
NH3 (g) + HCl (g) → NH4 Cl (s) ∆H0 = –176 kJ N2 (g) + 3H2 (g) → 2NH3 (g) ∆H0 = –92,2 kJ N2 (g) + 4H2 (g) + Cl2 (g) → 2NH4 Cl (s) ∆H0 = –628,9 kJ
Com base nas equações, é correto afirmar que a entalpia de reação de síntese do gás cloreto de hidrogênio é, em quilojoules, aproximadamente igual a:
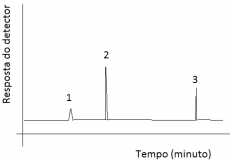
Com base em seus conhecimentos sobre a técnica, é possível afirmar que os compostos 1, 2 e 3 identificados pelo analista são, respectivamente:
