Questões de Concurso Público FURB - SC 2020 para Químico
Foram encontradas 13 questões
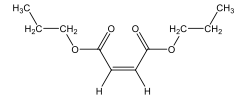
Figura - Estrutura química do dipropil maleato
A respeito da síntese e análise do dipropil maleato, assinale a alternativa correta:
( ) A principal região do espectro eletromagnético para identificação de compostos orgânicos é de 4000 a 400 cm-1 . ( ) Pode-se preparar pastilhas de KBr com amostras no estado sólido e líquido. ( ) Utilizando a técnica de ATR-FTIR, com um cristal de ZnSe, é possível obter espectros de filmes poliméricos, materiais oleosos e pós, na região entre 4000 a 400 cm-1 .
Assinale a alternativa com a sequência correta:
I- A técnica permite a quantificação de qualquer estrutura química, mesmo que não ocorra a formação de íons. II- Comumente os espectrômetros de massas são encontrados acoplados a um cromatógrafo líquido ou gasoso. III- A resolução na espectrometria de massa é definida como a capacidade de produzir dois sinais distintos para dois íons de massa atômica similar.
É correto o que se afirma em:
I- Dois tipos de eluição são empregados: isocrática (um único solvente) e gradiente (mistura de dois solventes). II- As colunas mais utilizadas na separação de compostos orgânicos são do tipo fase reversa com base de sílica com grupos C18 e C8. III- A fase móvel utilizada em HPLC são solventes de alto grau de pureza, como acetonitrila, hexano, metanol, água, entre outros.
É correto o que se afirma em:
Experimento [NH3] (mol L-1 ) [HNO3] (mol L-1 ) Velocidade da reação (mol L-1 s -1 ) 1 0,02 0,04 2.10-4 2 0,02 0,08 4.10-4 3 0,04 0,04 8.10-4
Baseado nos dados cinéticos, afirma-se:
I- A reação é de ordem 1 para o ácido nítrico. II- A reação é de ordem 2 para a amônia. III- A unidade da constante de velocidade é (mol L-1 ) s-1 .
É correto o que se afirma em:
I- Os valores de ka e pKa não podem ser utilizados de forma quantitativa, somente qualitativa. II- De maneira genérica, a constante de dissociação de um ácido em água pode ser escrita como Ka = ([A- ] [H3O+ ]) / ([HA] [H2O]). III- Quanto maior o valor de Ka, maior é a força do ácido.
É correto o que se afirma em:
3 Cuo(s) + 8 HNO3(aq) → 3 Cu(NO3)2(aq) + 2 NO(g) + 4 H2O(l) (1) 2 NO(g) + O2(g) → 2 NO2(g) (2) NO2(g) ⇌ N2O4(g) (3)
Isso posto, considerando um sistema transparente e fechado, o produto NO2(g) apresenta coloração marrom. O produto N2O4(g) é um gás incolor e, quando o sistema é aquecido acima da temperatura ambiente, o sistema apresenta uma coloração marrom (forte). Em relação à equação três, referente à formação do N2O4(g), é correto afirmar que:
O diagrama do orbital molecular do óxido de nitrogênio é confeccionado na seguinte ordem de distribuição dos orbitais moleculares: (σ1s, σ*1s, σ2s, σ*2s, σ2pz, π2px, π2py, π*2px, π*2py, σ*2pz
Com base no diagrama da molécula de óxido de nitrogênio, é correto afirmar que:
A respeito de um sistema adiabático, são dadas as seguintes sentenças:
I- A temperatura no interior do sistema adiabático é constante.
II- Em um processo de expansão adiabática, ocorre um aumento no volume e diminuição na pressão.
III- A energia interna, para um processo de compressão adiabática, é igual à soma das energias na forma de calor e do trabalho realizado sobre o sistema.
É correto o que se afirma em:
I- O ácido cianídrico pode ser utilizado como catalizador da reação. II- O mecanismo de reação pode ser descrito pela protonação do ácido acético, seguido de um ataque nucleofílico e pela eliminação de uma molécula de água. III- O mecanismo de reação pode ser descrito pela protonação do ácido acético, seguido de um ataque eletrofílico e pela eliminação de uma molécula de água.
É correto o que se afirma em: