Questões de Concurso Público SEED - RR 2021 para Professor de Educação Básica - Química
Foram encontradas 33 questões
Adaptado. Oxigênio Hospitalar (mixandi.com.br). Acesso em 24 de Julho de 2021.
Considere a seguinte situação hipotética. Temos em um hospital, um cilindro contendo gás oxigênio hospitalar com volume de 15 m3 , mantido à temperatura de -23 ℃ e à pressão de 25 atm. Assinale a alternativa que apresenta a quantidade, em mols, e a massa, em quilogramas (Kg), de O2 que estão contidas neste cilindro. Considere o O2 um gás ideal. Dados: R = 0,082 atm.L.K-1 .mol-1 ; M.M do gás O2 (g/mol) = 32.
I. O átomo era uma esfera não maciça, contendo carga elétrica positiva e negativa distribuídas em harmonia. O átomo teria carga elétrica total nula. II. O átomo não seria maciço como proposto por estudos anteriores. Seria descontínuo, nucleado e composto por duas regiões (O núcleo e a eletrosfera). III. O átomo era uma partícula minúscula, maciça, esférica e indivisível, não podendo ser criado nem destruído. IV. As órbitas elípticas indicaram um segundo número quântico (número quântico secundário), explicando como os espectros de emissão de luz apresentavam o fenômeno de linhas múltiplas nas raias espectrais. V. Os elétrons não giram aleatoriamente ao redor do núcleo, mas se movimentam ao redor do núcleo, em órbitas circulares determinadas. E cada órbita circular de elétrons apresentava um nível de energia definida e constante.
( ) Modelo de Dalton; ( ) Modelo de Thomson; ( ) Modelo de Rutherford; ( ) Modelo de Bohr; ( ) Modelo de Sommerfeld.
Assinale a alternativa que apresenta a sequência correta que associa os modelos atômicos aos seus respectivos responsáveis
A tabela periódica dos elementos químicos relaciona os elementos em linhas (Períodos) e colunas (Grupos ou Famílias), dispostos em ordem crescente de seus números atômicos. As propriedades dos elementos químicos presentes no mesmo grupo são semelhantes. Neste contexto, considere os seguintes elementos químicos e seus respectivos números atômicos.
Césio (Cs) Z = 55
Enxofre (S) Z = 16
Argônio (Ar) Z = 18
Magnésio Mg) Z =12
A partir dessas informações assinale a
alternativa correta.
Elementos Químicos Distribuição Eletrônica
I 1s2 2s2 2p6 3s23p3 II 1s2 2s2 2p6 3s2 3p6 4s2 3d8 III 1s2 2s2 2p6 3s2 3p6 4s2 IV 1s2 2s2 2p6 3s2 3p6 4s23d10 4p3 V 1s2 2s2 2p6 3s2 3p
De acordo com as informações localizadas na tabela acima, é correto afirmar que:
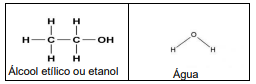
Após observar as fórmulas estruturais do etanol e da água, reconhecemos que o etanol se dissolve em água devido à formação de______:
Assinale a alternativa que preencha corretamente a lacuna.
Adaptado. Chapter 9 Molecular Geometries and Bonding Theories (ufpr.br). (Acesso em 23 de Julho de 2021).
Observe a tabela a seguir. E assinale a alternativa que apresenta a sequência que relaciona corretamente a substância ou o íon à sua geometria molecular, respectivamente.
Substâncias/íons Geometria Molecular I. NH3 ( ) Angular II. PH4+ ( ) Linear III. H2O ( ) Tetraédrica IV. CO2 ( ) Piramidal
Dados: Números atômicos (Z) H = 1; C = 6; N = 7; O = 8; P =15.
Adaptado.https://www.embrapa.br/documents/1355126/49258452/e mbrapa.br-Corre%C3%A7%C3%A3o+do+Solo+- +Portal+Embrapa.pdf/8a01a49d-0b94-c4e4-ea38- 5682ceb37955. (Acesso em 23 de Julho de 2021).
O processo de calagem do solo citado anteriormente no texto refere-se à utilização de calcário (CaCO3) para diminuir a acidez dos solos. Assim, quando o carbonato de cálcio é adicionado ao solo, ele pode reagir de vários modos. Assinale a alternativa que apresenta as equações químicas que podem ocorrer neste processo.
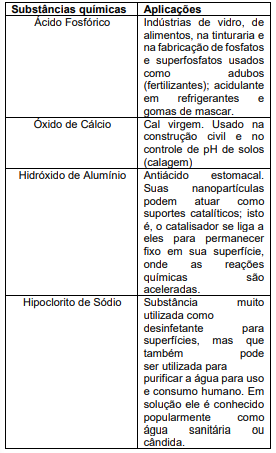
Assinale a alternativa que apresenta as fórmulas químicas que representam as substâncias presentes na tabela acima.
- O ar expelido pelos pulmões do suspeito é bombeado em uma solução de dicromato de potássio fortemente acidulada (ácido sulfúrico); - O etanol presente na boca do motorista (se este consumiu bebida alcoólica) reage com os íons dicromato da solução, produzindo acetaldeído e íons Cromo (III); - Em razão da reação química, ocorre uma mudança na cor da solução, a cor característica laranja passa para um tom esverdeado, acusando a presença de álcool etílico ou etanol.
Adaptado. Composição química do Bafômetro - Mundo Educação (uol.com.br). (Acesso em 23 de Julho de 2021)
A reação que ocorre no bafômetro com dicromato de potássio está representada pela equação química não balanceada a seguir:
K2Cr2O7(aq) + x H2SO4(aq) + 3CH3CH2OH(g) → alaranjado incolor
Cr2(SO4)3(aq) + y H2O(l) + 3CH3CHO(g) + K2SO4(aq) verde incolor
Assinale a alternativa que relaciona a classificação e os respectivos valores de x e y (mínimos coeficientes inteiros) que balanceiam corretamente a reação do bafômetro com dicromato de potássio.
Adaptado. Pilhas e Baterias de Lítio. Pilha e Baterias de íon lítio (uol.com.br). (Acesso em 23 de Julho de 2021).
Com relação à pilha de lítio usada em marca-passos e as transformações nela ocorridas, assinale a alternativa correta.
Adaptado.Produção de Alumínio: Extração da Bauxita, Obtenção na Eletrólise (culturalivre.com). (Acesso em 24 de Julho de 2021).
Podemos resumir a reação de obtenção do alumínio a partir do óxido de alumínio por meio da seguinte equação química balanceada. 2 Al2O3 (l) + 3 C(s) → 4 Al (l) + 3 CO2 (g) Dados: Massas atômicas (g/mol) Al=27; C=12; O=16. Assinale a alternativa que apresenta a massa, em gramas, de alumínio produzida se tivermos o triplo da quantidade, em mol, de óxido de alumínio e carvão.
Neste trecho da música do Emicida, a preocupação com o uso dos recursos naturais é notória. E nos faz refletir sobre as questões ambientais e suas implicações tecnológicas, sociais e científicas que fazem parte da nossa vida pessoal e profissional. Sendo assim, assinale a alternativa que apresenta quais problemáticas ambientais podemos relacionar ao trecho da música Passarinhos, de Emicida.
- O gás é formado por moléculas que se encontram em movimento desordenado e permanente. Cada molécula pode ter velocidade diferente das demais. - Cada molécula do gás interage com as outras somente por meio de colisões (forças normais de contato). A única energia das moléculas é a energia cinética. - Todas as colisões entre as moléculas e as paredes do recipiente que contém o gás são perfeitamente elásticas. A energia cinética total se conserva, mas a velocidade de cada molécula pode mudar. - As moléculas são infinitamente pequenas. A maior parte do volume ocupado por um gás é espaço vazio.
Seguindo estes quatro postulados, Boltzmann e Maxwell mostraram a relação entre a energia cinética média do total de moléculas de um gás ideal e sua temperatura conforme a expressão:
PV = 2/3 N { ½ m[v 2 ]} ½ m[v 2 ] = 3/2 kT Onde: N = número de moléculas; k (constante de Boltzmann) = 1,38.10 -23 J/K; T = temperatura absoluta (Kelvin)
Considere que o gás seja ideal, mantido em um recipiente isolado e fechado hermeticamente, e assinale a alternativa correta de acordo com a teoria cinética dos gases.
I. Estimular a instalação de equipamentos que monitoram e diminuem a toxicidade dos gases que são lançados na atmosfera por diversas indústrias pode reduzir a precipitação de chuvas ácidas. II. Evitar a liberação de monóxido de carbono que reage com a água, formando ácido carbônico, um dos principais responsáveis pelo aumento da acidez das chuvas, pode dificultar a precipitação de chuvas ácidas. III. Diversificar a matriz energética por meio da oferta e do uso de fontes renováveis ou alternativas de energia, diminuindo o lançamento de gases na atmosfera resultantes da queima de combustíveis fósseis pode inibir a precipitação de chuvas ácidas. IV. Dificultar a chegada da chuva ácida ao solo, evitando a neblina, que é o principal formato úmido da chuva ácida, responsável pela contaminação e desgaste dos solos, pode amenizar os efeitos negativos da precipitação ácida sobre as plantações.
Estão corretas as afirmativas:
Observe a tabela a seguir. Temos quatro reações (I, II, III e IV) e seus respectivos produtos.
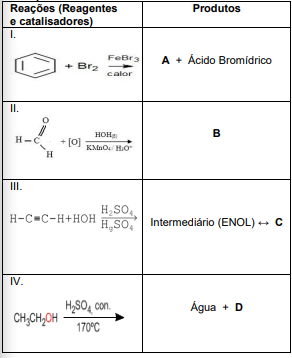
Analise as reações (I, II, III e IV) representadas
na tabela acima. Observe suas características
e sua classificação. Assinale a alternativa que
relaciona corretamente a reação e seu
respectivo produto (A, B, C e D),
respectivamente.
Os polímeros são grandes moléculas que apresentam unidades que se repetem, chamadas monômeros. Tais moléculas podem ser encontradas na natureza ou produzidas em laboratório, através de reações de polimerização. Uma das principais e mais importantes características dos polímeros é a resistência mecânica. E segundo ela, os polímeros podem ser divididos em termoplásticos, termoendurecíveis (termofixos) e elastômeros (borrachas). Um exemplo de plástico termofixo são as resinas epóxi. Elas são base para diversas aplicações e produtos industriais, sendo empregadas na fabricação de tintas, materiais compósitos, adesivos de engenharia de alta performance, fabricação de aviões, automóveis, bicicletas, barcos, snowboards, colagem de madeiras, metais, vidros e pedras, sob condições ambientais de temperatura e pressão. Além da fabricação de circuitos eletroeletrônicos, pois são protetores de componentes de pequenos circuitos, como resistores, transistores e capacitores.
Adaptado. g5.pdf (unicamp.br). Acesso em 25 de Julho de 2021.
A seguir, apresentamos a sua fórmula
estrutural.
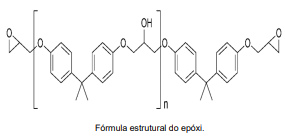
Analisando a fórmula estrutural do epóxi, assinale a alternativa correta.
Adaptado. CÉLULA A COMBUSTÍVEL, COMO FUNCIONA – Autoentusiastas. Acesso em 20 de Julho de 2021.
A seguir, temos um esquema da célula a combustível de gás hidrogênio.
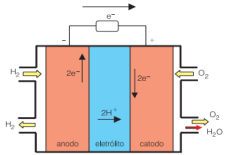
Esquema da célula a combustível de gás hidrogênio. Disponível em: www.usp.br/portalbiossistemas/?p=4316#:~:text=Em outras palavras%2C nessa célula a combustível a,célula a combustível é%3A H2 %2B ½O2→ H2O. Acesso em 20 de Julho de 2021.
A reação global balanceada da célula a combustível de gás hidrogênio é:
H2 (g) + ½O2 (g) → H2O (g)
Analisando o esquema da célula a combustível de gás hidrogênio (acima) e sua reação global balanceada, assinale a alternativa correta.
Adaptado. Sala BioQuímica: Controle (e descontrole) do pH sanguíneo (salabioquimica.blogspot.com). Acesso em 25 de Julho de 2021.
A seguir, temos as reações de conversão do gás carbônico (CO2) em bicarbonato (HCO3 - ).
CO2 (g) + H2O (l) ↔ H2CO3 (aq) H2CO3 (aq) ↔ HCO3 – (aq) + H+ (aq)
Elas são a base para entendermos o comportamento desse sistema tamponado do sangue nos dois ambientes diferentes: no tecido muscular e nos alvéolos. Assim, de acordo com as características do controle de pH do sistema sanguíneo, assinale a alternativa correta.