Questões de Concurso Público IF-ES 2023 para Técnico de Laboratório/Área: Química
Foram encontradas 50 questões
Pode-se obter o bórax anidro (Na2B4O7) através da reação representada pela equação não balanceada:
Ácido bórico + Metaborato de sódio → Na2B4O7 + H2O
A alternativa que apresenta as fórmulas corretas dos reagentes utilizados para sintetizar o bórax é:
CLASSIFICAÇÃO DE PERIGO DO PRODUTO (ABNT NBR 14725-2)
Mutagenicidade em células germinativas (Categoria 2)
Carcinogenicidade (Categoria 1B)
Toxicidade reprodutiva (Categoria 2)
ELEMENTOS APROPRIADOS DA ROTULAGEM (ABNT NBR 14725-3)
Pictogramas:

Palavra de Advertência: Perigo
Frases de Perigo:
341 Suspeito de provocar anomalias genéticas.
H350 Pode provocar cancro.
H361 Suspeito de afetar a fertilidade ou o nascituro.
Frases de Precaução:
P201 Pedir instruções específicas antes da utilização.
P202 Não manuseie o produto antes de ter lido e percebido todas as precauções de segurança.
P281 Usar o equipamento de proteção individual exigido.
P308 + P313 EM CASO DE exposição ou suspeita de exposição: consulte um médico.
P405 Armazenar em local fechado à chave.
P501 Eliminar o conteúdo/ recipiente em instalação aprovada de destruição de resíduos.
Portanto, quando ao técnico for solicitado o preparo de uma solução de fenolftaleína, os seguintes equipamentos devem ser utilizados, EXCETO:
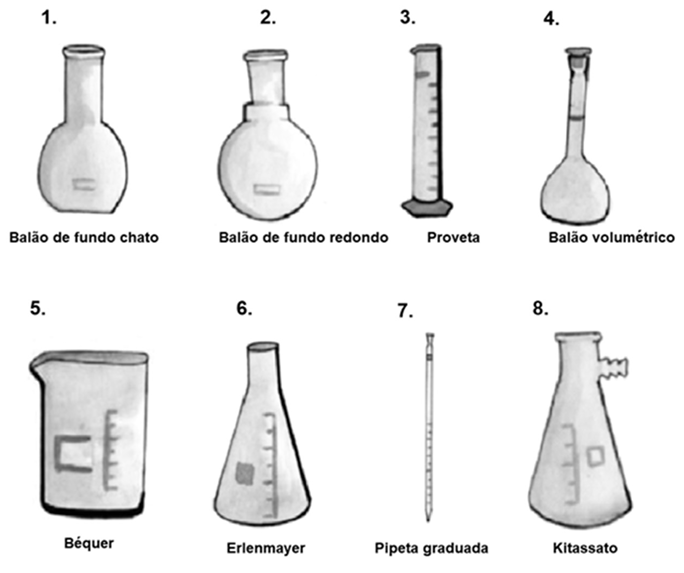
Fonte: Silva et al., 2019.
C2O4 2 – + MnO4 1 – + H + → Mn 2 + + H2O + CO2
Após o balanceamento correto, a soma dos coeficientes estequiométricos dos produtos da reação é:
Dado: Ka (HA) = 2,5.10 − 4 mol.L− 1
Concentração de Fosfato (μmol.L – 1 ) Absorbância (A) 5,00 0,08 10,0 0,16 20,0 0,33 40,0 0,65 50,0 0,81
Uma determinada amostra, ao ser analisada, apresentou absorbância de 0,57. Utilizando os dados da curva de calibração acima, a concentração de fosfato encontrada é: