Questões de Concurso Público IF-SP 2024 para Professor EBTT - Química
Foram encontradas 40 questões
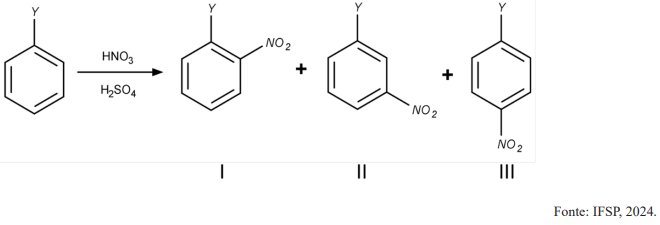
Com base nisso, assinale a alternativa correta:
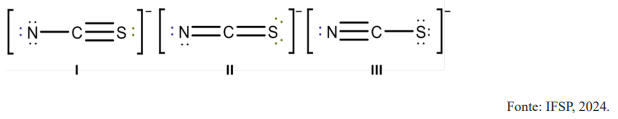
Assinale a alternativa que apresenta, em ordem crescente, a importância de cada estrutura para a composição do íon tiocianato:
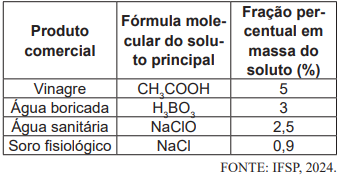
Uma pessoa possui, em sua casa, exatamente 100 mL de cada um dos produtos comerciais da tabela acima. Considerando os valores da fração percentual em massa do soluto na tabela acima, que a densidade de todas as soluções químicas é de 1,0 g mL-1 e que as soluções são formadas exclusivamente pelo soluto principal presente em água, escolha a alternativa que representa a menor concentração molar (mol L-1) do soluto em água.
Dados: H = 1,0 g mol-1; B = 10,8 g mol-1; C = 12,0 g mol-1; O = 16,0 g mol-1; Na = 23,0 g mol-1; Cl = 35,5 g mol-1
CaCO3(s) → CaO(s) + CO2(g)
A produção da cal virgem gera gás carbônico, um gás conhecido pelo seu papel na intensificação do efeito estufa. Qual o volume aproximado, nas CNTP, de gás carbônico produzido a partir da decomposição térmica de 250 kg de carbonato de cálcio? Utilize as massas molares (g mol-1) dos elementos C = 12, O = 16 e Ca = 40. Considere o rendimento da reação igual a 100 %, o comportamento do gás é ideal e a constante dos gases R = 0,082 atm L mol-1 K-1.
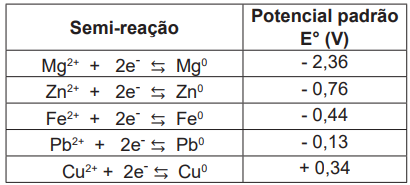
Fonte: JONES, L.; ATKINS, P. Princípios de Química: Questionando a vida moderna e o meio ambiente. 5. Ed. Porto Alegre: Bookman, 2012. p.532.
Os metais adequados para proteger essas peças metálicas contra a corrosão são:
Frasco A: REAÇÃO A : H2(g) + I2(g) ⇌ 2HI(g)
Frasco B: REAÇÃO B: 2NO2(g) ⇌ 2NO(g) + O2(g)
Considere os gases como ideias.
Se o volume de cada frasco for reduzido para um terço do volume inicial, é possível observar que:
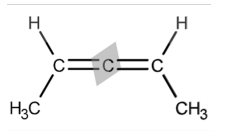 Fonte: IFSP, 2024.
Fonte: IFSP, 2024.Considerando a molécula da imagem acima e seu conhecimento em Química Orgância, é possível afirmar corretamente que
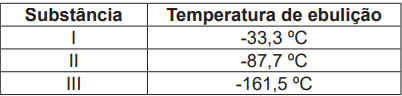
Fonte: ATKINS, P.; JONES, L.; LAVERMAN, L. Princípios de Química: Questionando a vida moderna e o meio ambiente. 7. ed. Porto Alegre: Bookman, 2018. p.191.
Considerando a relação existente entre as interações intermoleculares e a temperatura de ebulição, e comparando a temperatura de ebulição das três substâncias, assinale a alternativa que identifica, corretamente, a fórmula química das substâncias I, II e III. São dados os números atômicos dos elementos químicos H (Z=1), C (Z=6), N (Z=7) e P (Z=15).
CO(g) + CI2(g) → COCI2(g)
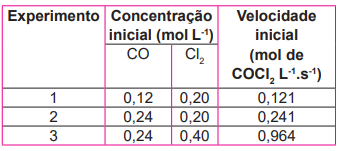
Dados:
Considere que a constante dos gases ideais (R) seja igual a 8 J·mol-1·K-1 e que lnK = -
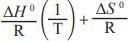
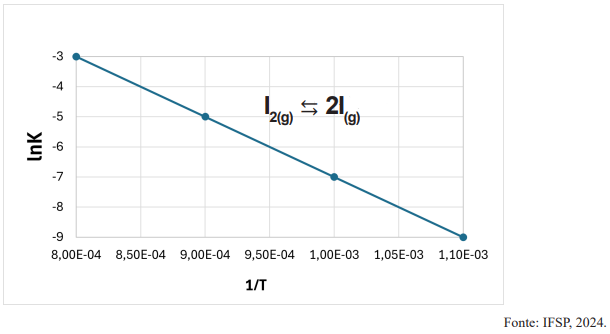
Com base nessas informações, é correto afirmar que:
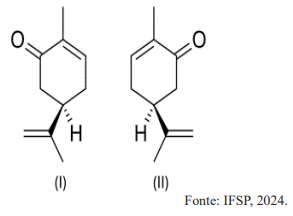
Com base nessas informações, é correto afirmar que:
Com relação aos conceitos de acidez e de chuva ácida, é correto afirmar que: