Questões de Concurso Público IF-TO 2021 para Professor EBTT - Química
Foram encontradas 50 questões
“A plataforma do Instituto Nacional de Meteorologia (Inmet) que monitora as maiores temperaturas registradas no Brasil a cada 24h, mostra que cinco cidades do Tocantins estavam entre as 10 mais quentes do Brasil nesta quinta-feira (26/8)”.
(Disponível em: https://afnoticias.com.br/estado/um-sol-pra-cada-um-5-cidades-do-tocantins-ficam-no-top-10-das-mais-quentes-do-pais. Acessado em 28/09/2021)
Em um estado tão quente quanto o Tocantins, buscamos alternativas para amenizar o calor, como as piscinas. Porém, é necessário mantê-las limpas para uso. Durante o tratamento da água da piscina é utilizado o sulfato de alumínio Al2 (SO4)3.
A obtenção de sulfato de alumínio se dá pela reação do alumínio sólido (Al) com o ácido sulfúrico (H2SO4 ). Considerando os dois reagentes puros, nas condições normais de temperatura e pressão (CNTP), qual o volume, em litros, de gás formado durante a preparação de 114 g de Al₂ (SO₄ )₃?
(Disponível em: https://jovempan.com.br/noticias/brasil/gas-de-cozinha-atinge-maior-preco-em-2021-e-deve-ficar-ainda- mais-caro-entenda-o-reajuste-da-petrobras.html. Acessado em 28/09/2021)
Supondo que todo o GLP presente no botijão seja somente butano e está totalmente na forma líquida, e que o preço do botijão de gás seja de R$ 125,00, para uma família que teve um gasto mensal com a fatura de gás de R$ 55,77, qual a quantidade de energia que foi liberada, em quilojoules, na queima do gás butano?
A reação de combustão completa do butano (não balanceada):
C₄H₁₀(g) → CO₂ (g) + H₂O ∆H°C = 2.808 kJ/mol
O dióxido de nitrogênio (NO₂ ) é uma molécula intermediária na produção industrial de ácido nítrico (HNO₃ ), que é muito aplicado na produção de fertilizantes. O dióxido de nitrogênio existe em equilíbrio com o tetróxido de nitrogênio (N₂O₄ ), segundo a reação:
2NO₂(g) ⇄ N₂O₄(g) ∆H = −57,23 kJ/mol
Para aumentar o rendimento do dióxido de
nitrogênio na reação, segundo o princípio de Le
Châtelier, deve-se:
I. A equação
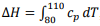 , pode ser usada para
calcular a variação da entalpia associado ao
aquecimento de um mol da substância. II. Se a substância for um líquido ou sólido, o
processo de aquecimento terá praticamente o
mesmo gasto energético a volume constante e
a pressão constante.
III. Se a substância for um gás ideal, o processo de
aquecimento a pressão constante gastará mais
energia que o processo de aquecimento a
volume constante.
, pode ser usada para
calcular a variação da entalpia associado ao
aquecimento de um mol da substância. II. Se a substância for um líquido ou sólido, o
processo de aquecimento terá praticamente o
mesmo gasto energético a volume constante e
a pressão constante.
III. Se a substância for um gás ideal, o processo de
aquecimento a pressão constante gastará mais
energia que o processo de aquecimento a
volume constante. Assinale a alternativa que contém a análise correta.
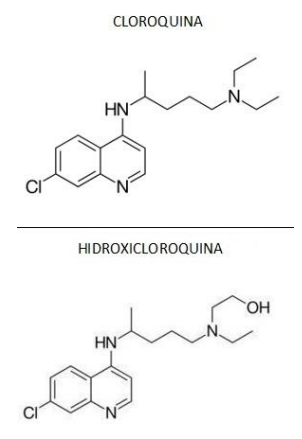
Quimicamente, a cloroquina (CQ) e a hidroxicloroquina (HCQ) pertencem à classe das 4- aminoquinodinas. Elas têm estrutura central aromática comum, com um cloro na posição 7, ligada às respectivas cadeias laterais básicas. A forma molecular da cloroquina é: C18H26CIN3, com massa molar de 319,9 g/mol. Já a hidroxicloroquina tem massa molar de 335,9 g/mol.
A CQ e a HCQ são administradas como difosfato e sulfato, respectivamente, em suas formas racêmicas.
Sobre o medicamento citado acima, marque o que
for correto.