Questões de Concurso Público UFMG 2018 para Químico II
Foram encontradas 30 questões
( ) As vidrarias não devem ser estocadas junto aos reagentes, pois podem ser contaminadas. ( ) Produtos não identificados devem ser armazenados em prateleiras abertas e ventiladas, longe de produtos inflamáveis. ( ) Produtos com data de validade vencida devem ser utilizados basicamente para testes de rotina. ( ) Reagentes explosivos e inflamáveis devem ser armazenados em lugares altos, dificultando o acesso de pessoas não autorizadas.
Em relação a essas normas, a sequência CORRETA é
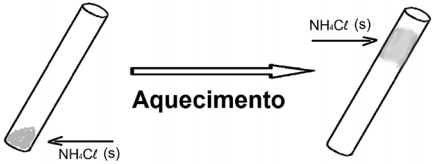
Com base nas observações do experimento, é CORRETO concluir que, nas condições em que o experimento foi realizado, o NH4 Cl

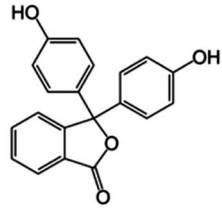
Em relação à figura, leia as seguintes afirmativas.
1. I é OM π ligante. 2. II é OM σ ligante. 3. III é OM π ligante. 4. IV é OM π antiligante.
Em relação a essas afirmativas, está CORRETA

Abaixo está representado o ciclo de Born-Haber para o cloreto de sódio sólido.
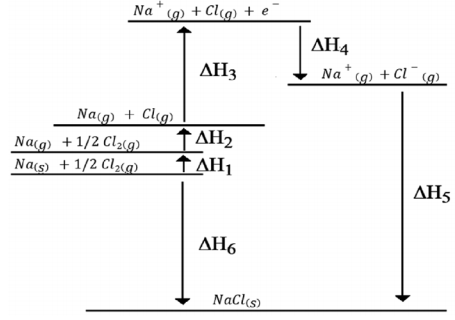
Qual das seguintes alternativas NÃO identifica corretamente a etapa correspondente na ilustração:
Replicatas Estudante A Estudante B 1 32,35 31,0 2 33,60 31,5 3 34,55 32,0 4 31,05 31,5
Considerando os valores mostrados na tabela é CORRETO afirmar que
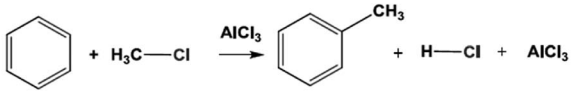
I – Nesta reação, o clorometano e o benzeno atuam como bases de Lewis. II – Neste processo, um par de elétrons π forma uma ligação química com o eletrófilo, promovendo a formação de uma carga positiva no interior do anel benzênico. III – Todas as etapas desta reação envolvem reações ácido-base. IV – O cloreto de alumínio tem basicamente duas funções: preparar o eletrófilo e recuperar a aromaticidade do anel.
Em relação a essas afirmativas, estão CORRETAS
Acerca dessas semirreações, considere as afirmações a seguir:
I – A reação acontecerá de forma espontânea entre Fe3+ e MnO4 - na proporção estequiométrica de 5 para 1. II – O potencial padrão para a reação global será 2,28 V. III – Em uma titulação entre as duas espécies, o potencial do ponto de equivalência será apenas dependente dos potenciais padrão das semirreações e do pH do meio. IV – O íon permanganato é um agente redutor mais fraco que o íon hidrogênio.
Em relação a essas afirmativas, estão CORRETAS
n-propanona 56,05 21,01 benzeno 80,09 2,28 n-propanol 97,20 20,80 isobutanol 107,89 17,93 n-butanol 117,73 17,84 n-pentanol 137,98 15,13
I – A ordem de eluição será de acordo com as temperaturas de ebulição, ou seja, n-propanona, benzeno, n-propanol, isobutanol, n-butanol e n-pentanol, que é diferente daquela que seria obtida com uma coluna apolar. II – Se, ao invés da temperatura constante fosse utilizada uma programação linear de temperatura, a ordem de eluição seria alterada. III – A constante dielétrica fornece uma medida aproximada da polaridade da molécula. IV – Se, ao invés da temperatura constante fosse utilizada uma programação linear de temperatura, o tempo de retenção seria certamente diferente dos obtidos no modo isotérmico.
De acordo com os dados fornecidos, estão INCORRETAS as informações
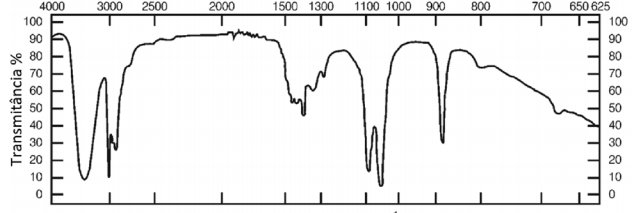 Número de onda (cm -1 ) De acordo com a análise do espectro, é CORRETO afirmar que o composto é
Número de onda (cm -1 ) De acordo com a análise do espectro, é CORRETO afirmar que o composto éI – Na absorção atômica, em chama, o analito deverá ser levado ao estado atômico gasoso. Após a atomização, o analito é levado ao estado excitado, tanto por absorção de energia térmica da chama quanto da radiação de frequência característica proveniente da lâmpada de cátodo oco. II – Na absorção atômica, em chama, o analito deverá ser levado ao estado atômico gasoso. Após a atomização, o analito é levado ao estado excitado somente por absorção de energia térmica da chama, não sendo excitado pela radiação de frequência característica proveniente da lâmpada de cátodo oco. III – Agente liberador é a espécie introduzida para combinar-se com o componente da amostra que iria apresentar interferência devido à formação de compostos de baixa volatilidade (refratários) com o analito. IV – Agente liberador é a espécie introduzida para combinar-se com o analito, a fim de liberá-lo da interferência que sofreria devido à formação de compostos de baixa volatilidade (refratários).
Em relação a essas afirmativas, estão CORRETAS