Questões de Concurso Público UFMG 2018 para Químico
Foram encontradas 12 questões
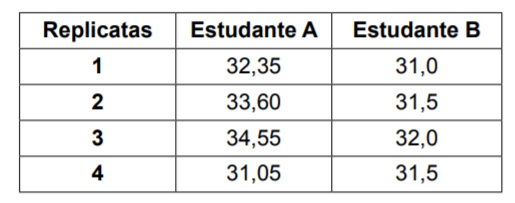
Considerando os valores mostrados na tabela é CORRETO afirmar que
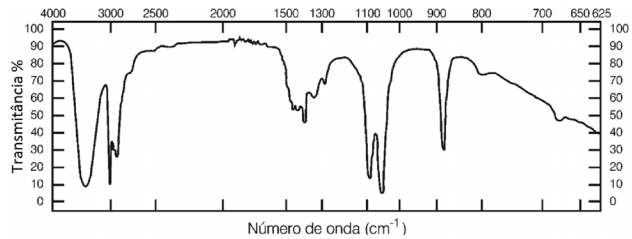
De acordo com a análise do espectro, é CORRETO afirmar que o composto é
Considere as seguintes afirmações com respeito à espectrometria atômica.
I – Na absorção atômica, em chama, o analito deverá ser levado ao estado atômico gasoso. Após a atomização, o analito é levado ao estado excitado, tanto por absorção de energia térmica da chama quanto da radiação de frequência característica proveniente da lâmpada de cátodo oco.
II – Na absorção atômica, em chama, o analito deverá ser levado ao estado atômico gasoso. Após a atomização, o analito é levado ao estado excitado somente por absorção de energia térmica da chama, não sendo excitado pela radiação de frequência característica proveniente da lâmpada de cátodo oco.
III – Agente liberador é a espécie introduzida para combinar-se com o componente da amostra que iria apresentar interferência devido à formação de compostos de baixa volatilidade (refratários) com o analito.
IV – Agente liberador é a espécie introduzida para combinar-se com o analito, a fim de liberá-lo da interferência que sofreria devido à formação de compostos de baixa volatilidade (refratários).
Em relação a essas afirmativas, estão CORRETA
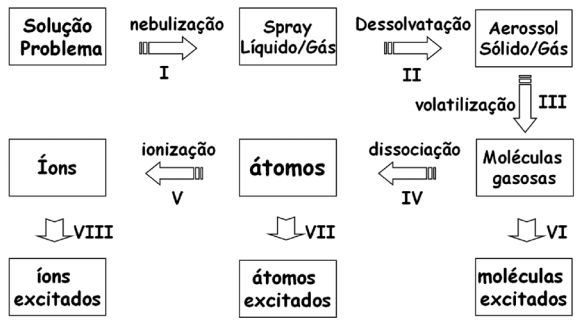
Considere o esquema e as seguintes afirmações:
I – A etapa IV é a responsável por produzir os átomos gasosos no estado fundamental. II – Na absorção atômica, utiliza-se um modulador, após a lâmpada, para eliminar os problemas que podem ser causados pela etapa VII. III – Somente a etapa V diminui a população de átomos gasosos no estado fundamental. IV – A etapa VII é indesejável para a absorção atômica, por diminuir a população de átomos gasosos no estado fundamental, porém é uma etapa essencial da espectrometria de emissão atômica.
Em relação a essas afirmativas, estão CORRETA
Nas alternativas a seguir estão apresentados problemas associados a uma explicação correta acerca desses problemas, EXCETO:
Com relação à interferência de ionização é CORRETO afirmar que
I - o supressor de ionização é um sal que contém um metal facilmente ionizável, que, ao se ionizar reduz a temperatura da chama, impedindo a ionização do analito. II - a supressão da ionização se dá pelo deslocamento de equilíbrio gerado pelo aumento da pressão parcial de elétrons na chama, após a ionização do supressor. III - a interferência de ionização é multiplicativa. Quando observada em uma curva de calibração, acarreta um coeficiente angular mais baixo, do que o obtido após a adição do supressor de ionização. IV - os elementos de fácil ionização, como os metais alcalinos, podem apresentar essa interferência, mesmo em chamas de acetileno/ar.
Em relação a essas afirmativas, estão CORRETAS:
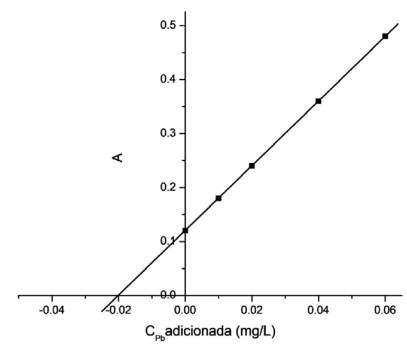
Com base nos resultados, o teor de chumbo da amostra de tequila analisada é:
IO3– + I– + H+ ⇆ I2+ H2O (produção de iodo) I2+ S2O32– ⇆ S4O62– + I– (titulação do iodo formado)
Para a resolução desta questão, estas equações deverão ser balanceadas.
Nesse processo, cada milimol de iodato, após adicionada a solução de iodeto, consumirá