Questões de Concurso Público UFMG 2022 para Técnico de Laboratório - Química
Foram encontradas 35 questões
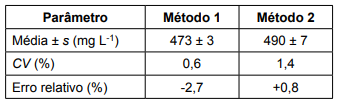
Com base nos dados apresentados, assinale a alternativa que apresenta uma análise CORRETA sobre os métodos utilizados.

Com base nesses dados, analise as afirmativas abaixo e assinale a INCORRETA.
I. A força da fase móvel aumenta quando o solvente se torna menos polar.
II. O pico de um composto mais polar terá tempo de retenção maior do que o de um composto menos polar.
III. A resolução entre dois picos cromatográficos tende a aumentar com o aumento do comprimento da coluna.
Assinale a alternativa com as afirmativas CORRETAS.
Veja abaixo a estrutura molecular de três dos mais comuns polímeros utilizados ̶ o PLA, o ABS e o PET:
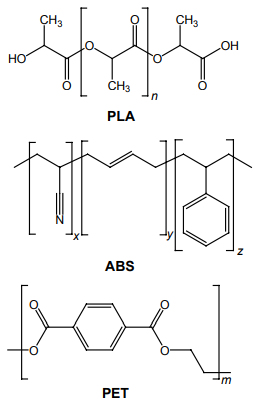
Sobre os polímeros, analise as afirmações abaixo:
I. O ABS é um copolímero constituído de três monômeros que podem se ligar de forma aleatória.
II. Tanto o PLA quanto o PET são polímeros que não resistem a meio básico, pois podem sofrer reações de hidrólise.
III. Os três polímeros possuem átomos quirais.
Assinale a alternativa que contém a(as) afirmativa(s) CORRETA(S).
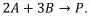
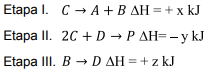
Assinale a alternativa que apresenta a expressão algébrica CORRETA para a variação de entalpia (∆H) da reação global.
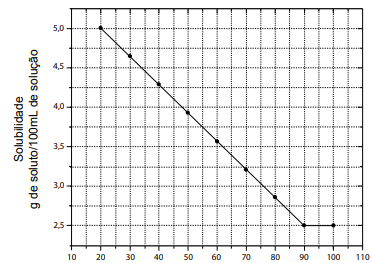 Temperatura /°C
Temperatura /°CCom base nesses dados, assinale a alternativa que indica o valor da constante do produto de solubilidade (KPS) do MnSO4 a 70 ºC.
( ) Ácido nítrico e ácido acético podem ser armazenados em um mesmo frasco de resíduo por apresentarem compatibilidade química.
( ) As tubulações de água, gases e ar comprimido devem apresentar cores diferentes.
( ) Um pictograma que indica que um determinado produto é oxidante traz como precaução: evitar atrito, choque, fricção, formação de faísca e ação de calor.
( ) Os extintores contendo gás carbônico são eficientes para extinguir incêndios causados por combustíveis líquidos e em equipamentos elétricos energizados.
Assinale a sequência CORRETA.
Assinale a alternativa em que está associada a região do espectro eletromagnético utilizada para realização das espectroscopias focadas em, respectivamente, vibrações moleculares e excitações eletrônicas por métodos de absorção de fótons.
Assinale a alternativa que contém o estado de oxidação do metal de transição das espécies apresentadas no texto, na ordem em que foram citados.
Com base nesses dados, assinale a alternativa que mostra o valor da constante Kc para essa reação.
Assinale a alternativa que contém, respectivamente, as concentrações dos íons cálcio e cloreto na solução diluída.
I. Na técnica de absorção atômica, os átomos da amostra absorvem parte da radiação proveniente de uma lâmpada e a luz não absorvida alcança o detector. A absorbância de um elemento químico, que é proporcional à sua concentração, pode ser determinada experimentalmente para cada pico referente ao elemento.
II. Na técnica de emissão atômica, nenhuma fonte de radiação precisa ser utilizada. A temperatura da chama e as colisões promovem os átomos da amostra a estados excitados que emitem fótons espontaneamente ao retornarem ao estado fundamental. A intensidade de emissão de um elemento químico é proporcional à sua concentração.
III. No experimento de fluorescência atômica, os átomos da amostra são irradiados com um laser e promovidos a estados excitados a partir do qual eles podem fluorescer para retornarem ao estado fundamental. Como esse processo envolve transições não-radiativas, a intensidade de emissão de um elemento não deve ser usada para determinar sua concentração.
Assinale a alternativa que contém as afirmativas CORRETAS.
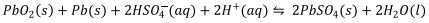
Dados: E° red (cátodo) = + 1,685 V e E° red (ânodo) = - 0,356 V
Analise as afirmações numeradas de I a IV em relação a esse tipo de bateria.
I. Os eletrodos de PbO2(s) e Pb(s) são inertes, sendo o potencial de pilha dependente apenas da concentração de ácido sulfúrico.
II. No processo de recarga da bateria ocorre redução do pH do meio aquoso.
III. O Pb(s) atua como agente redutor no processo de recarga da bateria.
IV. O processo de descarga leva a um potencial padrão de pilha de +2,041 V e a uma redução da densidade do eletrólito.
Assinale a alternativa CORRETA.
Ag+(aq) + I- (aq) → AgI(s) Ag+(aq) + SCN- (aq) → AgSCN(s)
Sabendo que o volume de KSCN gasto na titulação foi de 5,00 mL, assinale a alternativa que indica corretamente o teor de KI por comprimido.